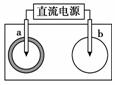
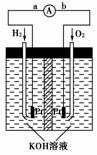
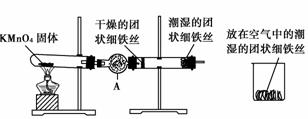
11.铁及铁的化合物应用广泛,如FeCl3可用做催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式是
________________________________________________________________________。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。
正极反应________________,负极反应__________________。
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10 mol·L-1,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤_______________
________________________________________________________________________。
|
|
氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
Fe3+ |
1.9 7.0 4.7 |
3.2 9.0 6.7 |
|
Fe2+ |
||
|
Cu2+ |
||
|
提供的药品:Cl2 浓H2SO4 NaOH溶液 CuO Cu |
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀。
有关反应的化学方程式____________________________________________________
________________________________________________________________________。
劣质不锈钢腐蚀的实验现象________________________________________________。
[解析] (1)该反应是FeCl3氧化金属铜,离子方程式为2Fe3++Cu===2Fe2++Cu2+
(2)将(1)中反应设计成原电池必须是Cu作负极,选择比铜不活泼的金属或碳棒为正极,FeCl3溶液作电解质溶液。装置图如右图所示:
正极:2Fe3++2e-===2F e2+
e2+
负极:Cu-2e-===Cu2+
(3)根据表给出的数据可知,把Cu2+中混有的Fe2+、Fe3+除掉的方法是将Fe2+氧化为Fe3+,调节溶液的pH到3.2-4.7,Fe3+以Fe(OH)3的形式沉淀,过滤除去,根据除杂原则,去杂不能加杂,选择氧化剂为Cl2,加入CuO调节溶液的pH。
(4)根据题给条件,此不锈钢在盐溶液中腐蚀明显,可选择的药品为CuO、浓H2SO4,先用水稀释浓H2SO4再用H2SO4与CuO反应生成CuSO4溶液,不锈钢与CuSO4溶液反应,在不锈钢的表面有紫红色物质生成,即可验证劣质不锈钢易被腐蚀。
[答案] (1)2Fe3++Cu===2Fe2++Cu2+
(2)装置图如下

正极反应:Fe3++e-===Fe2+(或2Fe3++2e-===2Fe2+)
负极反应:Cu===Cu2++2e-(或Cu-2e-===Cu2+)
(3)①通入足量氯气将Fe2+氧化成Fe3+;
②加入CuO调节溶液的pH至3.2-4.7;
③过滤[除去Fe(OH)3]
(4)CuO+H2SO4===CuSO4+H2O
CuSO4+Fe===FeSO4+Cu
不锈钢表面有紫红色物质生成

 Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2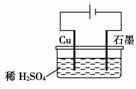 某同学按下图所示的装置进行电解实验。下列说法正确的是
某同学按下图所示的装置进行电解实验。下列说法正确的是