16.(14分)镁是一种轻金属,其合金的强度高、机械性能好。这些特性使金属镁成为制造汽车、飞机、火箭的重要材料,从而获得“国防金属”的美誉。海水矿物质中镁的浓度仅次于氯和钠,居第三位。由于对镁的需求非常巨大,很多沿海国家都建有大型海水提镁工厂。
下表是有关物质的Ksp:
|
物质 |
CaCO3 |
MgCO3 |
Ca(OH)2 |
Mg(OH)2 |
|
溶度积 |
2.8×10-9 |
6.8×10-6 |
5.5×10-6 |
1.8×10-11 |
回答下列问题:
(1)能否直接把贝壳研磨成粉末,撒入海水中使Mg2+转化为MgCO3沉淀,其原因是_________________________________________________________________________________。
(2)实际生产中是把Mg2+转化为Mg(OH)2沉淀,而不是转化为MgCO3沉淀,其理由是________________________________________________________________________;
请你推测应将贝壳进行怎样的加工处理_________________________________________________________________________________。
(3)某同学在实验室条件下模拟该生产过程,在加试剂时,误将纯碱溶液加入海水中,他思考了一下,又在得到的混合体系中加入过量的烧碱溶液,你觉得他________(填“能”或“不能”)将Mg2+转化为Mg(OH)2沉淀,理由是_________________________________________________________________________________。
(4)过滤出Mg(OH)2沉淀后,用试剂________(填化学式)将其溶解,选择该试剂的理由是____________________________________
________________________________________________________________________。
[解析] (1)CaCO3和MgCO3化学式所表示的组成中阴、阳离子个数比相同,从Ksp看,CaCO3的溶解能力比MgCO3的小,所以不能直接加贝壳粉末使Mg2+转化为MgCO3沉淀;
(2)MgCO3的溶度积比Mg(OH)2的溶度积大,所以应把Mg2+转化为Mg(OH)2沉淀,即把贝壳研磨、煅烧、加水制成石灰乳[Ca(OH)2];
(3)根据沉淀的转化,烧碱电离产生的OH-能结合MgCO3溶解产生的Mg2+生成溶解度更小的Mg(OH)2沉淀,使MgCO3的溶解平衡不断向右移动;
(4)盐酸电离的H+与Mg(OH)2溶解产生的OH-生成水,使Mg(OH)2的溶解平衡不断右移。
[答案] (1)不能,MgCO3的溶解度比CaCO3溶解度大,直接加贝壳粉末得不到MgCO3沉淀
(2)为使Mg2+沉淀完全,应将Mg2+转化为溶解度更小的Mg(OH)2 研磨、煅烧、加水制成石灰乳
(3)能 烧碱电离产生的OH-能结合MgCO3溶解产生的Mg2+生成溶解度更小的Mg(OH)2沉淀,使MgCO3的溶解平衡不断向右移动
(4)HCl 盐酸电离的H+与Mg(OH)2溶解产生的OH-生成水,使Mg(OH)2的溶解平衡不断右移
13.(14分)有一个七只杯子魔术实验,非常有趣,杯中的试剂不同或试剂的量不同,通过发生氧化还原反应或酸碱反应,因pH及所用指示剂不同,而显示不同的颜色。七只杯子中的药品、实验步骤及转移次序如下图所示:
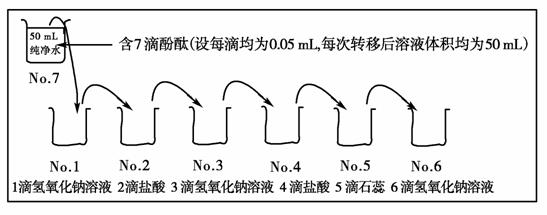
试回答下列问题:
(1)若盐酸和氢氧化钠溶液的浓度均为0.1 mol·L-1,1-5号杯子中依次出现的颜色是:
|
杯号 |
1 |
2 |
3 |
4 |
5 |
6 |
|
颜色 |
|
|
|
|
|
蓝紫色 |
当液体进入时,哪个杯中水的电离度最大?________(选填1-6号,下同);哪个杯中水的电离度最小?________。
(2)若2号杯显无色,4号杯显无色,5号杯显红色,则[NaOH]与[HCl]的关系是________________________________________________________________________。
[解析] (1)溶液进入1号杯时,[OH-]=0.1 mol·L-1×0.05×10-3 L÷(50×10-3 L)=10-4 mol·L-1,pH=10;进入2号杯时氢氧化钠被中和,且盐酸剩余,相当于过量1滴盐酸,此时溶液中[H+]=0.1 mol·L-1×0.05×10-3 L÷(50×10-3 L)=10-4 mol·L-1,pH=4;3号杯,[OH-]=2×10-4 mol·L-1,[H+]=5×10-11 mol·L-1,pH=10.3;4号及5号杯,[H+]=2×10-4 mol·L-1,pH=3.7;6号杯中,由于共用了NaOH溶液1+3+6=10滴,共用了盐酸2+4=6滴,相当于过量了4滴NaOH溶液,[OH-]为1号溶液的4倍,即[OH-]=4×10-4 mol·L-1,[H+]=2.5×10-11 mol·L-1,pH=10.6。由于H+和OH-能同等程度抑制水的电离,故水的电离度最大的是1号和2号,此时由水电离的[H+]或[OH-]为10-10 mol·L-1;水的电离度最小的是6号,水电离的[H+]或[OH-]为2.5×10-11 mol·L-1。
(2)由于2号杯显无色,说明pH<8即[OH-]<10-6 mol·L-1;由于4号和5号溶质相同,4号显无色,说明pH<8,5号显红色,说明是石蕊显色,pH<5,即[H+]>10-5 mol·L-1。设盐酸和NaOH溶液的物质的量浓度分别为a mol·L-1、b mol·L-1,在2号杯中,应用(0.05b-2×0.05a)÷50<10-6,即b<2a+0.001,在5号杯中,(6×0.05a-4×0.05b)/50>10-5,求得b<1.5a-0.002 5,故综合起来,有b<1.5a-0.002 5。
[答案] (1)红色 无色 红色 无色 红色 1号和2号 6号
(2)[NaOH]<1.5[HCl]-0.002 5 mol·L-1
 HS-+H+,HS-
HS-+H+,HS- Al3++3OH-;Al(OH)3+H2O
Al3++3OH-;Al(OH)3+H2O [Al(OH)4]-+H+
[Al(OH)4]-+H+
 H2CO3+OH-的水解平衡____________________________________________________________________________________________________________________________(要求写出简要操作,现象及实验能说明的问题)。
H2CO3+OH-的水解平衡____________________________________________________________________________________________________________________________(要求写出简要操作,现象及实验能说明的问题)。 H++A2-。现有下列四种溶液:
H++A2-。现有下列四种溶液: H2A+OH-
H2A+OH- HCN+OH-,故已水解的[CN-]=[OH-]=10-2 mol·L-1,水解率为10-2
mol·L-1/0.1 mol·L-1×100%=10%,故A正确;NH4CN显碱性说明水解程度CN->NH4+,从而说明NH3·H2O比HCN易电离,故B正确;C不正确,高氯酸铵是强酸弱碱盐,水溶液显酸性,[H+]>[OH-];D正确,加入KOH可抑制Na2S水解。
HCN+OH-,故已水解的[CN-]=[OH-]=10-2 mol·L-1,水解率为10-2
mol·L-1/0.1 mol·L-1×100%=10%,故A正确;NH4CN显碱性说明水解程度CN->NH4+,从而说明NH3·H2O比HCN易电离,故B正确;C不正确,高氯酸铵是强酸弱碱盐,水溶液显酸性,[H+]>[OH-];D正确,加入KOH可抑制Na2S水解。