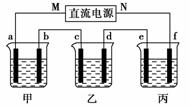
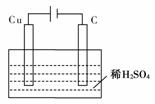
15.如下图所示,p、q为直流电源两极,A为+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D产生气泡。试回答:
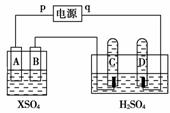
(1)p为____极,A极发生了________反应。
(2)C为______极,试管里收集到________;D为______极,试管里收集到________。
(3)C极的电极方程式是______________________________。
(4)在电解过程中,测得了C、D两极上产生的气体的实验数据如下:
|
时间(min) |
1 |
2 |
3 |
4 |
5 |
|
阴极生成气体体积(cm3) |
6 |
12 |
20 |
29 |
39 |
|
阳极生成气体体积(cm3) |
2 |
4 |
7 |
11 |
16 |
|
时间(min) |
6 |
7 |
8 |
9 |
10 |
|
阴极生成气体体积(cm3) |
49 |
59 |
69 |
79 |
89 |
|
阳极生成气体体积(cm3) |
21 |
26 |
31 |
36 |
41 |
仔细分析以上实验数据,请说出可能的原因是____________。
(5)当反应进行一段时间后,A、B电极附近溶液的pH______(填“增大”“减小”或“不变”)。
(6)当电路中通过0.004 mol电子时,B电极上沉积金属X为0.128 g,则此金属的摩尔质量为________。
[解析] (1)接通电源,X沉积于B极,说明B为阴极,则A为阳极,故(1)中q为负极,p为正极,A上发生氧化反应。(2)H2SO4电解池中,C为阳极,C试管内得O2,D为阴极,此试管内得H2。
(4)C、D两极所得O2、H2体积应该为1∶2,但实验数据由1∶3随时间变化而增大,到达10分钟时约为1∶2,因为开始O2溶解的原因。
(5)A极:X―→X2++2e-。B极:X2++2e-―→X,两极附近pH不变。
(6)设X的摩尔质量为M g/mol,则
X2++2e-―→X
2 mol M g