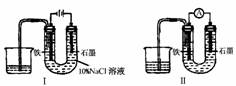
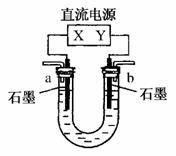
10.(2010·江西省联考)用下图装置(X、Y是直流电源的两极)分别进行下列各组实验,则下表中所列各项对应关系均正确的一组是( )
|
选项 |
电源X极 |
实验前U形管中液体 |
通电后现象及结论 |
|
A |
正极 |
Na2SO4溶液 |
U形管两端滴入酚酞试液后,a管中呈红色 |
|
B |
正极 |
AgNO3溶液 |
b管中电极反应式是4OH--4e-===2H2O+O2↑ |
|
C |
负极 |
KCl和CuCl2混合溶液 |
相同条件下,a、b两管中产生的气体总体积可能相等 |
|
D |
负极 |
Fe(OH)3胶体和导电液 |
b管中液体颜色加深 |
解析:X为正极,电解Na2SO4溶液时,实质是电解水,a管中电极为阳极,OH-放电,a管中c(H+)>c(OH-),滴加酚酞试液不变色,A错;X为正极,电解AgNO3溶液时,b管中电极为阴极,电极反应式为Ag++e-===Ag,B错;Fe(OH)3胶体粒子带有正电荷,X为负极时,Fe(OH)3胶体粒子向a管移动,a管中液体颜色加深,D错。
答案:C

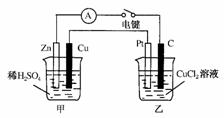
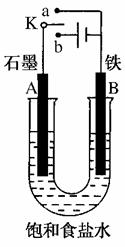
 NiOOH+MH,下列叙述正确的是( )
NiOOH+MH,下列叙述正确的是( )