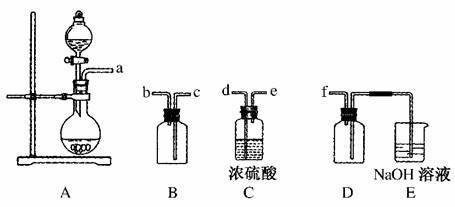
14.(2010·唐山市联考)教材中经常利用如图装置进行有关物质的制备和性质检验。

(1)请按要求填充下表空格:
|
实验名称 |
选用的仪器(填字母) |
C或D中所盛试剂(填名称) |
C或D中的现象 |
|
区别固体Na2CO3和NaHCO3 |
BD |
澄清石灰水 |
|
|
铜和浓硫酸反应 |
AC |
|
溶液红色褪去 |
|
制备乙酸乙酯 |
|
饱和碳酸钠溶液 |
上层有透明油状液体产生并有香味 |
(2)针对上述实验下列说法正确的是(填写字母代号)________。
A.Cu和浓硫酸反应时,可在装置C的试管口塞沾有碱液的棉花
B.加热装置C中已吸收Cu和浓硫酸反应生成物后的溶液不能出现红色
C.制备乙酸乙酯时,装置C的导管末端在液面以下
D.装置B可用于制备氨气
解析:(1)碳酸氢钠受热分解产生二氧化碳,二氧化碳遇澄清石灰水生成白色的CaCO3沉淀而使澄清石灰水变浑浊;根据现象“溶液红色褪去”及铜与浓硫酸反应的产物可知加入的试剂为品红溶液;实验室中制备乙酸乙酯的反应物为液体,所以选用装置A作为反应器,用装置C作为产物乙酸乙酯的接收装置及除杂装置。
(2)铜与浓硫酸反应容易逸出有毒气体二氧化硫,该气体可以溶解在碱液中,所以可以用沾有碱液的棉花吸收,A正确;品红溶液吸收二氧化硫生成不稳定的无色物质,加热可以释放出二氧化硫,品红溶液恢复红色,B错;为了防止倒吸,制备乙酸乙酯时,装置C的导管不能插入吸收液中,C错;装置B是加热固体反应物的装置,故可以加入铵盐与碱的混合物制备氨气,D正确。
答案:(1)
|
|
|
|
|
|
|
|
|
澄清石灰水变浑浊 |
|
|
|
品红溶液 |
|
|
|
AC |
|
|
(2)AD
12.(2010·武汉市武昌区调研)某无色溶液中含有:①Na+、②Ba2+、③Cl-、④Br-、⑤SO、⑥SO中的一种或几种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
|
步骤 |
操作 |
现象 |
|
① |
用pH试纸检验 |
溶液的pH大于7 |
|
② |
向溶液中滴加氯水,再加入CCl4振荡,静置 |
CCl4层呈橙色 |
|
③ |
向②所得溶液中加入Ba(NO3)2溶液和稀HNO3 |
有白色沉淀产生 |
|
④ |
过滤,向滤液中加入AgNO3溶液和稀HNO3 |
有白色沉淀产生 |
下列结论正确的是( )
A.肯定含有的离子是①④⑤
B.肯定没有的离子是②⑤
C.可能含有的离子是①②⑥
D.不能确定的离子是①③⑥
解析:根据步骤②,说明加入氯水后有Br2生成,则原溶液中一定含有Br-;根据步骤③,说明步骤②所得溶液中有SO,则原溶液中至少含有SO、SO中的一种;步骤④,说明步骤②、步骤③所得溶液中有Cl-,由于步骤②中加入氯水引入了Cl-,则不能确定原溶液中是否含有Cl-;结合①,溶液显碱性,则一定含有SO,SO无法确定;由于Ba2+不能与SO、SO共存,则原溶液中一定不含Ba2+,根据电荷守恒,则原溶液中一定含有Na+。因此肯定含有的离子是①④⑤,肯定没有的离子是②,不能确定的离子是③⑥。
答案:A
11.(2010·邯郸市摸底考试)用试纸检验气体性质是一种重要的实验方法。如图所示的实验中(可加热),下列试纸的选用、现象、对应结论都正确的一项是( )

|
选项 |
试剂B |
湿润的试纸A |
现象 |
结论 |
|
A |
碘水 |
淀粉试纸 |
变蓝 |
碘具有氧化性 |
|
B |
浓氨水,生石灰 |
蓝色石蕊试纸 |
变红 |
氨气为碱性气体 |
|
C |
Na2SO3,硫酸 |
品红试纸 |
褪色 |
SO2具有漂白性 |
|
D |
Cu,浓硝酸 |
KI淀粉试纸 |
变蓝 |
NO2为酸性气体 |
解析:选项A,碘水中的I2与淀粉作用出现蓝色,与I2的氧化性无关。选项B,NH3遇红色石蕊试纸变蓝,证明NH3是一种碱性气体。选项C,Na2SO3与H2SO4反应产生SO2,SO2使品红试纸褪色,证明SO2具有漂白性。选项D,Cu与浓HNO3反应产生NO2,NO2氧化I-生成的I2与淀粉作用变蓝,证明NO2具有氧化性而不是酸性。
答案:C
 (3)焰色反应
(3)焰色反应