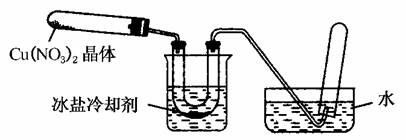
(1)反应中最先起氧化作用的是________。
(2)该探究小组对反应后溶液中铁元素的价态进行探究,他们设计了实验方案,并进行实验。请按下表格式补充写出实验操作步骤、预期现象与结论。
|
实验操作步骤 |
预期现象与结论 |
|
步骤1:观察样品 |
溶液呈蓝绿色,________(填“能”或“不能”)确定产物中铁元素的价态 |
|
步骤2:取少量溶液,滴加酸性KMnO4溶液 |
|
|
步骤3:________ |
若溶液变为红色,说明产物中含+3价的铁元素;若溶液颜色无明显变化,则说明产物中不含+3价的铁元素 |
解析:(一)(1)由反应3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O与3CuO+6HNO3(稀)===3Cu(NO3)2+6H2O相比,生成等物质的量的Cu(NO3)2前者消耗HNO3多,而且生成的NO污染空气。
(2)固体的灼烧应放在坩埚中进行;从溶液中得到硝酸铜晶体应先蒸发浓缩再冷却结晶,最后过滤。
11.(2010·黄冈市质检)某同学用NaHCO3和KHCO3组成的混合物进行实验,测得实验数据(盐酸的物质的量浓度相等)如下表:
|
盐酸/mL |
50 |
50 |
50 |
|
混合物质量/g |
9.2 |
15.7 |
27.6 |
|
标准状况下CO2体积/L |
2.24 |
3.36 |
3.36 |
下列分析推理不正确的是( )
A.盐酸的物质的量浓度为3.0 mol/L
B.根据表中数据能计算混合物中NaHCO3的质量分数
C.加入9.2 g混合物时盐酸过量
D.15.7 g混合物恰好与盐酸完全反应
解析:A项,由表中数据可知,求盐酸浓度需选择盐酸不足量的数据进行,如随着混合物质量增加,二氧化碳气体量不再增加,表明盐酸全部反应完,H++HCO-3=H2O+CO2↑,c(HCl)=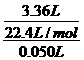 =3 .0 mol/L,正确;B项,根据表中第一栏数据固体混合物的总质量及产生标准状况下的二氧化碳气体的体积可以计算出NaHCO3的质量分数,正确;C项,由于固体混合物从9.2 g→15.7 g,二氧化碳气体的体积还在增加,故盐酸过量,正确;D项,根据固体混合物与气体的比例关系可知,产生3.36 L二氧化碳所需固体质量为:
=3 .0 mol/L,正确;B项,根据表中第一栏数据固体混合物的总质量及产生标准状况下的二氧化碳气体的体积可以计算出NaHCO3的质量分数,正确;C项,由于固体混合物从9.2 g→15.7 g,二氧化碳气体的体积还在增加,故盐酸过量,正确;D项,根据固体混合物与气体的比例关系可知,产生3.36 L二氧化碳所需固体质量为: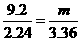 ,解得m=13.8 g,此时盐酸恰好完全反应,故不正确。
,解得m=13.8 g,此时盐酸恰好完全反应,故不正确。
答案:D
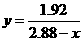 ,此时2.16g≤x<2.4g;另外,x=2.4 g时也符合
,此时2.16g≤x<2.4g;另外,x=2.4 g时也符合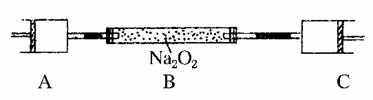
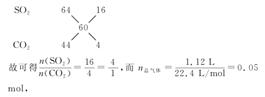
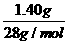 =0.05 mol,而C筒中气体体积无变化,则A中另一种气体为O2,n(O2)=
=0.05 mol,而C筒中气体体积无变化,则A中另一种气体为O2,n(O2)=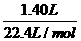 -0.05 mol=0.0125 mol,故A中气体的质量为:0.05 mol×44 g/mol+0.0125 mol×32 g/mol=2.6 g。
-0.05 mol=0.0125 mol,故A中气体的质量为:0.05 mol×44 g/mol+0.0125 mol×32 g/mol=2.6 g。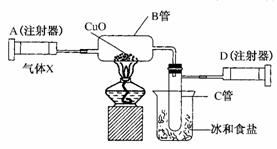
 =0.02 mol,n(N2)=
=0.02 mol,n(N2)= =0.01 mol,
=0.01 mol,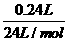 =0.01 mol,因此n(X):n(N):n(H)=0.01 mol:(0.01
mol×2):(0.02 mol×2)=1:2:4,所以X的化学式为N2H4,摩尔质量为32 g/mol。
=0.01 mol,因此n(X):n(N):n(H)=0.01 mol:(0.01
mol×2):(0.02 mol×2)=1:2:4,所以X的化学式为N2H4,摩尔质量为32 g/mol。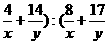 )=448:672,解得:x:y=1:2,只有C项符合。
)=448:672,解得:x:y=1:2,只有C项符合。