21.某研究性学习小组为了验证臭氧的氧化性强于氧气,进行了下述实验,请参与探究并回答相关问题。
[实验目的]验证臭氧的氧化性强于氧气。
[实验原理]2KI+O3+H2O===2KOH+I2+O2,淀粉溶液遇单质碘变蓝色。
[实验用品]臭氧消毒碗柜、a溶液、碘化钾溶液、滤纸、玻璃片、温度计。
[实验步骤]
①取a溶液与碘化钾溶液混合。
②取两片用滤纸剪成的纸条,在a和碘化钾的混合液中湿润后分别置于两块洁净的玻璃片上。
③将一块玻璃片(Ⅰ)置于臭氧消毒碗柜中并接通电源生成臭氧。将另一块玻璃片(Ⅱ)置于可控温度的温箱里,尽量地使温箱的温度与消毒碗柜中的温度相等。
④观察现象并进行记录:
|
时间(min) |
0 |
15 |
30 |
45 |
60 |
90 |
120 |
|
|
滤纸的 颜色变化 |
玻璃片(Ⅰ)上的滤纸 |
白色 |
白色 |
灰色 |
浅蓝色 |
蓝色 |
蓝色 |
浅蓝色 |
|
玻璃片(Ⅱ) 上的滤纸 |
白色 |
白色 |
白色 |
白色 |
灰色 |
灰色 |
浅蓝色 |
请根据上述实验原理、步骤及你所学的知识,回答下列问题:
(1)实验药品中的a溶液是__________溶液。
(2)写出在臭氧消毒柜中产生O3的化学方程式:______________________________。
(3)整个实验过程要保持两块玻璃片所在环境的温度相同的原因是______________________。
(4)从实验数据记录可以得出的结论是__________(填序号)。
A.O3的氧化性比O2强
B.氧气也能氧化碘化钾中的碘离子
C.空气中可能也有一定浓度的O3,所以实验数据不可靠,不能达到实验目的
D.O3不仅氧化I-的速率比氧气快,而且有漂白作用
(5)在O3氧化KI的反应中,若有9.6 g O3发生反应,则转移的电子的物质的量为__________。
答案:(1)淀粉 (2)3O2通电2O3
(3)温度会影响反应速率,保持温度相同是为了消除温度不同带来的误差
 国际奥委会公布的违禁药物目前有一百多种,某种兴奋剂的结构如图,关于它的说法正确的是 ( )
国际奥委会公布的违禁药物目前有一百多种,某种兴奋剂的结构如图,关于它的说法正确的是 ( )
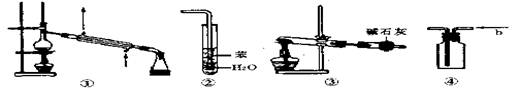 11、实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( ) ( )
11、实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( ) ( )