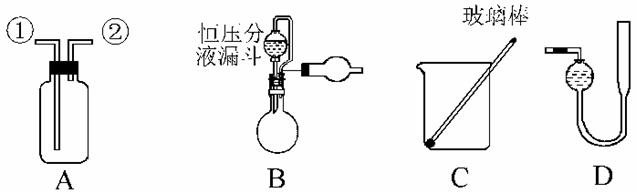
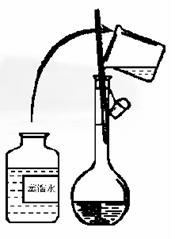
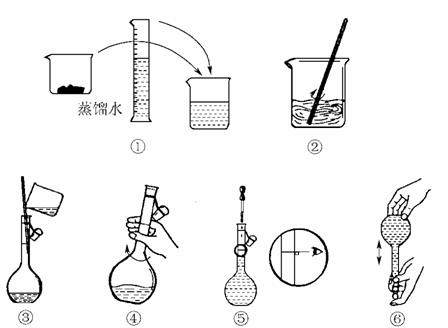
21.已知某白色粉末只有K2SO4、NH4HCO3、KCl、NH4Cl、CuSO4五种物质中的两种,为检验该白色粉末的成分,请完成下列实验:
实验一:取适量该白色粉末于烧杯中,加蒸馏水溶解,得到无色透明溶液A。将溶液A分成两份,分别装于两支试管中,向其中一支试管里滴加稀硝酸,有无色气泡产生。
由此判断,该白色粉末中肯定含有__________,肯定不含有__________。
实验二:
|
待检验物质 |
实验操作 |
预期现象和结论 |
|
K2SO4 |
向盛有溶液A的另一支试管中滴加__________溶液 |
|
实验三:
|
实验前提 |
实验操作 |
预期现象和结论 |
|
若白色 粉末中不 含K2SO4 |
取少量原固体混合物于试管中,用酒精灯充分加热 |
如果试管底部有固体残留,则混合物中含有________;如果试管底部无固体残留,则混合物中含有__________ |
答案:实验一:NH4HCO3 CuSO4
实验二:BaCl2 若出现白色沉淀,则含有K2SO4
实验三:NH4HCO3和KCl NH4HCO3和NH4Cl
19.某同学为了测定三聚氰胺的分子式,设计了如下实验:
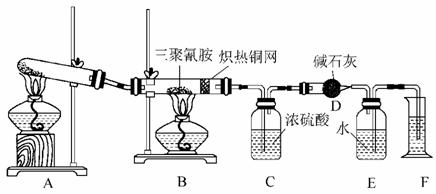
查阅资料,三聚氰胺的相对分子质量为126,三聚氰胺在常温下为晶体,在加热条件下能与氧气发生反应生成二氧化碳、氮气和水。取12.6 g三聚氰胺晶体按图示实验反应(假设三聚氰胺完全转化成产物)。
(1)写出A装置中发生反应的化学方程式________________________________________。
(2)C装置能不能与D装置互换?__________(填“能”或“不能”)。理由是____________________________。
(3)当B装置中反应完全发生后,读取F中水的体积的实验操作顺序为__________(填序号)。
①读数 ②冷却至室温 ③调平E、F装置中的液面
(4)测定数据如下:
|
装置 |
C |
D |
|
实验前 |
101.0 g |
56.0 g |
|
实验后 |
106.4 g |
69.2 g |
经测定,E中收集的气体折合成标准状况下的体积为6.72 L。
①利用上述实验数据,计算三聚氰胺的实验式为__________。
②三聚氰胺分子式为__________。
③若B装置中没有铜网,对测定结果的影响是__________________________________。
解析:(1)根据实验原理知:A装置用于制取氧气,且采用加热固体的方法制氧气;(2)碱石灰既能吸收二氧化碳又能吸收水,而浓硫酸只吸收水,不能吸收二氧化碳;(4)C装置增加的质量就是水的质量,D装置增加的质量就是二氧化碳的质量,n(CO2)=(69.2-56.0) g/44 g/mol=0.3 mol,n(H2O)=(106.4-101.0) g/18 g/mol=0.3 mol,n(N2)=6.72 L/22.4 L/mol=0.3 mol。则反应物中C、H、N元素的总质量=0.3 mol×12 g/mol+0.6 mol×1 g/mol+0.6 mol×14 g/mol=12.6 g,说明样品不含氧元素。所以三聚氰胺分子中,n(C)∶n(H)∶n(N)=0.3 mol∶0.6 mol∶0.6 mol=1∶2∶2,设三聚氰胺的分子式为(CH2N2)n,则(12+2+28)n=126,n=3,故其分子式为C3H6N6。若B装置中没有铜网,可能有没有反应的氧气进入E瓶中,导致测定的氮气体积偏大,即测定得到的三聚氰胺分子式中氮原子数偏大,而碳、氢原子数偏小。
答案:(1)2KMnO4△K2MnO4+MnO2+O2↑或2KClO3MnO2△2KCl+3O2↑ (2)不能 实验中浓硫酸吸收水,碱石灰吸收二氧化碳,若互换,碱石灰能同时吸收二氧化碳和水,导致实验失败 (3)②③① (4)CH2N2 C3H6N6 使测定所得的三聚氰胺分子式中氮原子数偏大,碳、氢原子数偏小