19.(2009·青岛)“碘钟”实验中,3I-+S2O===I+2SO的反应速率可以用I与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
|
实验编号 |
① |
② |
③ |
④ |
⑤ |
|
c(I-)/(mol·L-1) |
0.040 |
0.080 |
0.080 |
0.160 |
0.120 |
|
c(S2O)/(mol·L-1) |
0.040 |
0.040 |
0.080 |
0.020 |
0.040 |
|
t/s |
88.0 |
44.0 |
22.0 |
44.0 |
t1 |
回答下列问题:
(1)该实验的目的是_____________________________________________________。
(2)显色时间t1=________________________________________________________。
(3)温度对该反应的反应速度的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为__________(填字母)。
A.<22.0 s B.22.0 s-44.0 s
C.>44.0 s D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是____________。
解析:本题主要考查外部因素如浓度、温度对化学反应速率的影响。由已知数据可知,当c(I-)和c(S2O)乘积相等时,显色时间相等,即反应速率相等,但时间与速度成反比,故
t1==29.3 s。升高温度加快化学反应速率,即缩短显蓝色的时间,故t<22.0 s。
答案:(1)研究反应物I-与S2O的浓度对反应速率的影响 (2)29.3 s (3)A (4)反应速率与反应物起始浓度乘积成正比(或显色时间与反应物起始浓度乘积成反比)
18.(2009·宁夏)硫代硫酸钠溶液与稀硫酸反应的化学方程式为:
Na2S2O3+H2SO4===Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是
( )
|
实验 |
反应温度/℃ |
Na2S2O3溶液 |
稀H2SO4 |
H2O |
||
|
V/mL |
c/(mol·L-1) |
V/mL |
c(mol·L-1) |
V/mL |
||
|
A |
25 |
5 |
0.1 |
10 |
0.1 |
5 |
|
B |
25 |
5 |
0.2 |
5 |
0.2 |
10 |
|
C |
35 |
5 |
0.1 |
10 |
0.1 |
5 |
|
D |
35 |
5 |
0.2 |
5 |
0.2 |
10 |
解析:D与A、B比较,D温度高;D与C比较,溶液混合后体积相同,而D中n(Na2S2O3)比C中大。
答案:D
16.在一密闭容器中加入A、B、C三种气体,保持一定温度,在t1-t4(s)时刻测得各物质的浓度如下表。据此下列结论正确的是 ( )
|
测定时刻/s |
t1 |
t2 |
t3 |
t4 |
|
c(A)/mol·L-1 |
6 |
3 |
2 |
2 |
|
c(B)/mol·L-1 |
5 |
3.5 |
3 |
3 |
|
c(C)/mol·L-1 |
1 |
2.5 |
3 |
3 |
A.在t3时刻反应已经停止
B.A的转化率比B的转化率低
C.在容器中发生的反应为:2A+B===C
D.在t2-t3内A的平均反应速率为[1/(t3-t2)]mol/(L·s)
答案:D
 CO(g)+H2(g)
CO(g)+H2(g)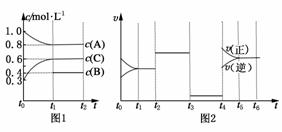
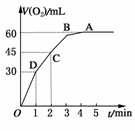

 N2(g)+2CO2(g)。下列说法不正确的是 ( )
N2(g)+2CO2(g)。下列说法不正确的是 ( )