10、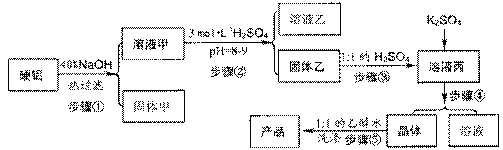 Ⅰ.硬铝废料(含90%铝、2.5%镁、7.5%铜)可以制取明矾KAl(SO4)2.12H2O,某探究小组设计了下列实验。
Ⅰ.硬铝废料(含90%铝、2.5%镁、7.5%铜)可以制取明矾KAl(SO4)2.12H2O,某探究小组设计了下列实验。
请回答以下问题:
(1)写出步骤③的离子方程式 。
(2)步骤④包括三个环节,分别是_______、冷却结晶、________。
(3)步骤⑤不直接用水洗的原因是_________________________。
 Ⅱ.某课题小组同学测量液态奶含氮量的实验过程如下:
Ⅱ.某课题小组同学测量液态奶含氮量的实验过程如下:
原理:
步骤:
① 在烧杯中加入10.00mL液态奶和辅助试剂,加热充分反应;
 ② 将反应液转移到大试管中;
② 将反应液转移到大试管中;
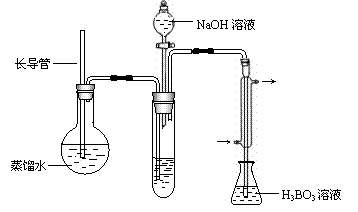
③ 按如下装置用水蒸气将NH3吹出,
并用H3BO3溶液吸收(加热装置未画出);
④ 取下锥形瓶,滴加指示剂,用0.1000 mol·L-1
盐酸标准液滴定;
⑤ 重复测定两次,再用10.00mL蒸馏水代替液态奶进行上述操作。
数据记录如下:
|
实验编号 |
样品和辅助试剂 |
消耗盐酸体积(mL) |
|
1 |
10.00mL液态奶、0.2g催化剂、20mL浓硫酸 |
33.45 |
|
2 |
10.00mL液态奶、0.2g催化剂、20mL浓硫酸 |
33.55 |
|
3 |
10.00mL液态奶、0.2g催化剂、20mL浓硫酸 |
33.50 |
|
4 |
10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸 |
1.50 |
回答下列问题:
(1)滴定时(NH4)2B4O7重新转化为H3BO3,反应的化学方程式为_____________________。
(2)步骤③的实验装置中需要加热的仪器是_____________(填仪器名称),长导管的作用是______________________________________ ___________。
(3)设计4号空白对照实验的目的是____________________________________________。
(4)计算该液态奶的含氮量为____________mg·mL-1。
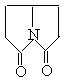

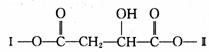
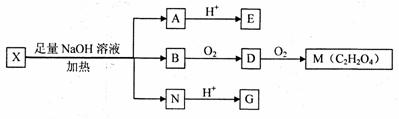 为推测X的分子结构,进行如下图的转化:
为推测X的分子结构,进行如下图的转化: FeO(s)+CO(g) 平衡常数为K1;
FeO(s)+CO(g) 平衡常数为K1;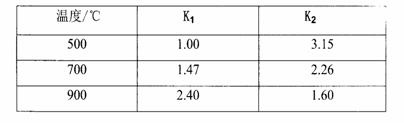
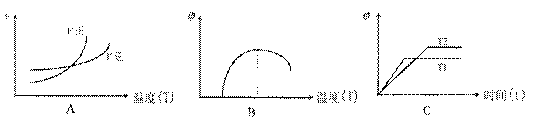

 已知一个B分子中含有的Z元素的原子个数比一个C分子中少一个。而W的单质在常温常压下为固体,并且W元素是形成化合物种类最多的元素。请回答下列问题:
已知一个B分子中含有的Z元素的原子个数比一个C分子中少一个。而W的单质在常温常压下为固体,并且W元素是形成化合物种类最多的元素。请回答下列问题: