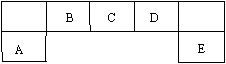1.(16分)下面是某同学检验海水中溴离子的实验,请你参与他的探究:
(1)由于溴离子在海水中浓度很低(0.067g/L),要先取海水样品(设取70mL)进行浓缩,浓缩时下面的仪器 是不需要的(填编号):
A.玻璃棒 B.三脚架 C.酒精灯 D.蒸发皿 E.100mL烧杯
(2)取浓缩后的海水(假设剩余10mL左右)进行氧化和萃取。
① 下列试剂都可以氧化浓缩后海水中的溴离子,实验中最好选 (填编号):
A.氯水 B.双氧水 C.酸性高锰酸钾溶液
②加入一定量氧化剂后,对氧化后的溶液进行假设和实验:
假设1:溶液中全部为Br-; 假设2:溶液全部为Br2
假设3:溶液中 。
③设计方案、进行实验,验证假设:请在表中写出实验步骤以及预期现象和结论(可以不填满)。限选实验试剂和仪器:10mL量筒、小烧杯、试管、胶头滴管、分液漏斗;无水乙醇、裂化汽油、苯、0.10mol/LAgNO3、0.10mol/LHNO3
|
实验步骤 |
预期现象和结论 |
|
步骤1:用量筒取样品溶液6mL于试管中,再取
|
若上层有机层出现橙色或橙红色,则假设2或假设3成立;
|
|
步骤2:将上述液体倒入
|
|
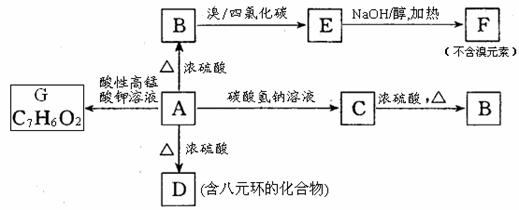
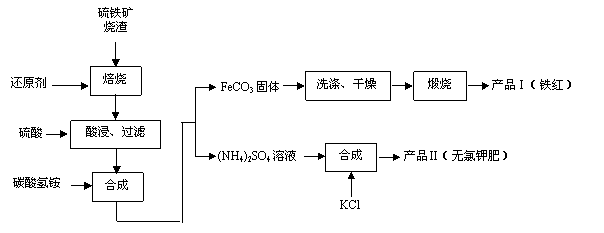

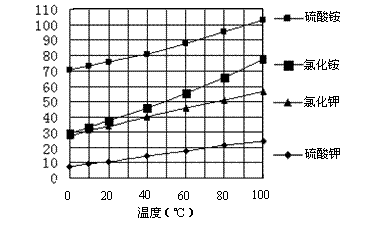

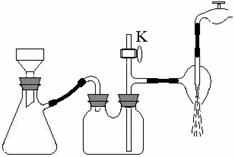 (3)分离粗产品Ⅱ时承接滤液的烧杯中应加入少量________,分离粗产品Ⅱ后的滤液冷却至室温后,进行减压抽滤,得粗产品Ⅲ。所用的装置如右图所示,若实验过程中发现倒吸现象,应采取的措施是 。
(3)分离粗产品Ⅱ时承接滤液的烧杯中应加入少量________,分离粗产品Ⅱ后的滤液冷却至室温后,进行减压抽滤,得粗产品Ⅲ。所用的装置如右图所示,若实验过程中发现倒吸现象,应采取的措施是 。
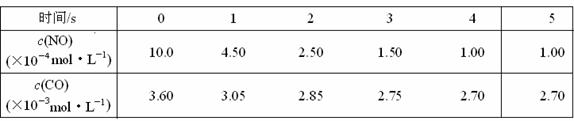

 下列说法错误的是 。
下列说法错误的是 。