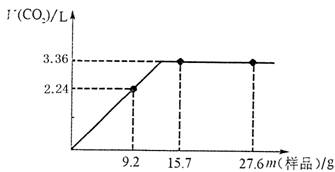
25.(16分)Na2SO3固体在空气中久置容易变质。
I请写出Na2SO3固体在空气中变质的化学方程式______________
Ⅱ实验室中欲检验 Na2SO3 固体样品是否已经变质,最简单的方法为______________
Ⅲ选用以下装置莉药品通过测定生成SO2的质量,可计算Na2SO3固体样品的纯度。
反应原理:H2SO4(浓)+ Na2SO3= Na2SO4 + SO2↑+ H2O
供选用的药品:①浓硫酸 ②浓硝酸 ③碱石灰 ④空气
供选用的装置(同一装置可重复选用):
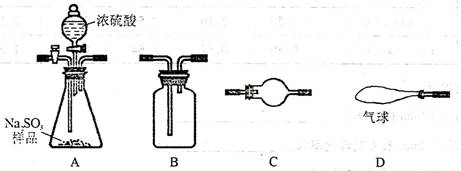
(1)将所选仪器按连接硕序从左至右依次填入下表,并对应填入该仪器中所加试剂 (不用填A 装置中的药品;根据需要填写,可不填满)
|
实验装置(填字母) |
D |
|
|
|
|
|
|
|
装置中所盛药品(填序号) |
④ |
|
|
|
|
|
|
(2)称取a gNa2S03固体样品,上述实验完成后,测得生成SO2的质量为5g则该Na2SO3固体祥品的质量分数为______________。
24.(12分)在恒温、恒容的密闭容器中,混合气体A、B、C 的物质的量浓度(c)与时间(t) 的关系如下表所示:
|
t c |
初始 |
2min |
4min |
6min |
8min |
|
c(A)(
mol·L
-1) |
2.50 |
2.20 |
2.00 |
2.00 |
2.20 |
|
c(B)(
mol·L
-1) |
1.56 |
2.16 |
2.56 |
2.56 |
2.16 |
|
c(C)(
mol·L
-1) |
0.39 |
0.54 |
0.64 |
0.64 |
1.54 |
请填空:
(1)前2mim内,v(B)= ______________。
(2) 到2mim末A 的转化率为______________
(3)该反应的化学方程式为____________________________
(4)6 min - 8 min若只改变了反应体系中某一种物质的浓度,则应为_____(填选项字母)
a.增大A的浓度 b.减小B的浓度 c.增大C的浓度
则该物质的浓度改变量为______________ mol·L -1
(5) 如果在相同条件下,要使该反应从逆反应方向开始进行 ,且达平衡时与第4min 时各物质的体积分数完全相同,则加入B 的物质的量浓度的取值范围为______________
 C.乙醇、甲苯、硝基苯 D.甲酸、乙醛、乙酸
C.乙醇、甲苯、硝基苯 D.甲酸、乙醛、乙酸