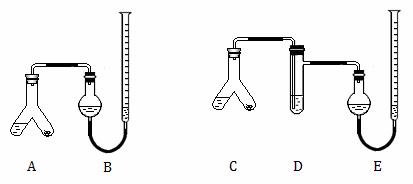
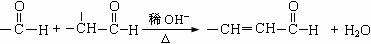27.(15分)煤的气化是高效、清洁地利用煤炭的重要途径之一。
(1)在25℃、101kPa时,H2与O2化合生成1 mol H2O(g)放出241.8kJ的热量,其热化学方程式为 。
又知:①C(s)+ O2 (g) ==== CO2 (g) ΔH =-393.5 kJ/mol
②CO(g) + 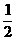 O2 (g) ==== CO2 (g) ΔH = -283.0 kJ/mol
O2 (g) ==== CO2 (g) ΔH = -283.0 kJ/mol
焦炭与水蒸气反应是将固体煤变为气体燃料的方法,C(s) + H2O(g) ==== CO(g) + H2(g) ΔH = kJ/mol。
(2)CO可以与H2O(g)进一步发生反应:CO(g) + H2O(g)  CO2(g)+H2(g) ΔH<0
CO2(g)+H2(g) ΔH<0
在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,在800℃时达到平衡状态,K=1.0。
|
起始物质的量 |
甲 |
乙 |
丙 |
|
n(H2O)/
mol |
0.10 |
0.20 |
0.20 |
|
n(CO)/
mol |
0.10 |
0.10 |
0.20 |
①该反应的平衡常数表达式为 。
②平衡时,甲容器中CO的转化率是 ;
容器中CO的转化率:乙 甲;丙 甲。(填“>”、“=”或“<”)
③丙容器中,通过改变温度,使CO的平衡转化率升高,则温度 (填“升高”或“降低”)。
 物对应的水化物碱性:X>Y>Z
物对应的水化物碱性:X>Y>Z
 不定项选择题:本题包括7小题,每小题4分,共计28分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。
不定项选择题:本题包括7小题,每小题4分,共计28分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。 2PbO+2SO2;
2PbO+2SO2; 下列装置或操作不能达到实验目的的是
下列装置或操作不能达到实验目的的是  下列有关说法或表示正确的是
下列有关说法或表示正确的是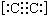 2-
2-
 。
。
 -CH2OCH2- + H2O
-CH2OCH2- + H2O