31、某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00mol/L、2.00mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO3的用量为25.00mL,大理石用量为10.00g。
(1)请完成以下实验设计表,并在实验目的一栏中填空:
|
实验 编号 |
温度 (℃) |
大理石 规格 |
HNO3浓度(mol/L) |
实验目的 |
|
① |
25 |
粗颗粒 |
2.00 |
(I)实验①和②探究浓度对反应速率的影响; (II)实验①和③探究温度对反应速率的影响; (III)实验①和④探究 对反应速率的影响 |
|
② |
|
|
|
|
|
③ |
|
|
|
|
|
④ |
|
|
|
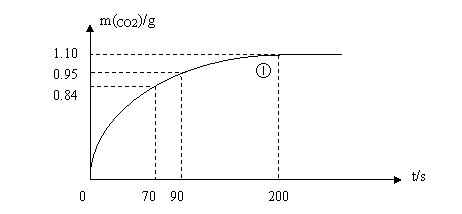
(2)实验①中CO2质量随时间变化的关系见下图。计算实验①中70s-90s
范围内用HNO3表示的平均反应速率 (忽略溶液体积变化,不需要写出计算过程)。

27、(10分)下表是元素周期表的一部分, 针对表中的①-⑨种元素,填写下列空白:
|
主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
|
2 |
|
|
|
① |
② |
③ |
|
|
|
3 |
④ |
|
⑤ |
|
|
⑥ |
⑦ |
⑧ |
|
4 |
⑨ |
|
|
|
|
|
|
|
(1) 在这些元素中,化学性质最不活泼的是: (用元素符号表示,下同)
(2) 在最高价氧化物的水化物中,酸性最强的化合物的分子式是_______,碱性最强的化合物的化学式是:_____________。
(3) 最高价氧化物是两性氧化物的元素是_____ ____;写出它的氢氧化物与氢氧化钠反应的离子方程式_____ _________ _________ _________ _________ ____。
(4) 用电子式表示元素④与⑥的化合物的形成过程: ,
该化合物属于 (填 “共价”或“离子”)化合物。
(5)表示①与③的化合物的电子式 ,
该化合物是由 (填“极性”“非极性”)键形成的。
 2C(g),经4 s后达到平衡状态,在相同温度下测得容器内混合气体的压强是反应前的5/6,
2C(g),经4 s后达到平衡状态,在相同温度下测得容器内混合气体的压强是反应前的5/6,  2NH3中,每生成2mol NH3, 热量(填:吸收或放出)
kJ; www.k@s@5@
高#考#资#源#网
2NH3中,每生成2mol NH3, 热量(填:吸收或放出)
kJ; www.k@s@5@
高#考#资#源#网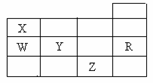 A.Y、Z的阴离子电子层结构都与R原子的相同
A.Y、Z的阴离子电子层结构都与R原子的相同