26、(9分)氧化铜在高温下发生分解反应:4CuO 高温 2Cu2O+O2↑,把一定量的氧化铜粉末在高温下加热使其部分分解,得到固体混合物(CuO、Cu2O),铜和氧的质量比用mCu:mO表示,请回答下列问题。
(1)上述固体混合物中mCu:mO不可能是:________(选填A、B、C,多选扣分)
A.16:2 B.16:3 C.16:4
(2)若所得的固体混合物中mCu:mO=16:a,计算CuO的分解率A%= %。
(3)如果CuO被H2还原分两步进行
|
|
2CuO+H2======Cu2O+H2O Cu2O+H2======2Cu+H2O
试分析反应后得到的固体混合物的可能组成,相应的mCu:mO=16:b,写出b的取值范围,将结果填入下表(不一定填满)。
|
混合物组成(用化学式表示) |
b的取值范围 |
|
|
|
|
|
|
|
|
|
|
|
|
高中毕业班第二次综合模拟考试
19.(6分)“过氧乙酸”是抗“非典”中广泛用于医院、地面、门窗、汽车等方面的消毒液。下面是市售过氧乙酸商品标签:
|
过氧乙酸 甲、乙溶液各500mL 用法:把本品甲溶液1份,乙溶液 1份在玻璃或塑料容器内混合放24 小时,即可稀释使用 |
技术要求 含量不少于10%,一般可以用50倍纯水稀释使用(浓度为0.2%) |
(1)配制过氧乙酸消毒液的甲、乙溶液的主要成分各是什么?某校研究性学习小组为此进行以下研究,请你完成下列相关内容:
1查阅资料:过氧乙酸消毒液是由H2O2、H2O、CH3COOH及少量H2SO4混合后,反应生成过氧乙酸(CH3COOOH)为主要消毒成份的溶液。CH3COOOH容易放出原子氧,它与空气中微生物机体作用,达到灭菌目的。H2O2在酸性介质中稳定,是一种强氧化剂。
2提出假设:__________________________________________________________。
3实验验证:
|
实验主要步骤 |
实验主要现象 |
|
|
|
4得出结论:__________________________________________________________。
(2)该校根据“非典”消毒要求,急需配制0.2%过氧乙酸消毒液1m3,需要购进甲溶液_________瓶,乙溶液____________瓶。
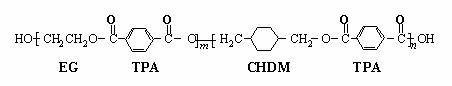
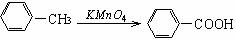
 RCOOR2 +R1OH (R、R1、R2表示烃基)
RCOOR2 +R1OH (R、R1、R2表示烃基)