16.(7分)A-G是几种烃的分子球棍模型,据此回答下列问题
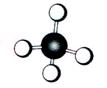
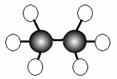
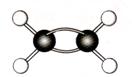
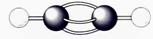
A B C D
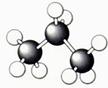
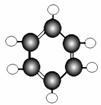
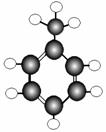
E F G
(1)常温下含碳量最高的气态烃是 ;
(2)能够发生加成反应的烃有 种;
(3)一卤代物种类最多的是(填对应字母) ;
(4)写出实验室制取C的化学方程式 ;
(5)写出F发生溴代反应的化学方程式 。
17 (9分)A、B、C和D代表原子序数依次增大的四种短周期元素,它们满足以下条件:①C的原子序数是A、B的原子序数之和,A、C、D的最外层电子数之和为13;②D的原子序数是C的2倍,D的最高价氧化物对应的水化物是二元强酸。请填空:
(1)A是 元素, D单质形成的晶体属于 (填晶体类型);
(2)B单质的电子式为 ,画出C元素的原子结构示意图 ;
(3)写出一个由B单质转化为其化合物的化学方程式: ;
(4)已知:由A、B、C、D 四种元素组成的两种化合物在水溶液中反应可生成一种无色有刺激性气味的气体,则这两种化合物都是由 键构成,试写出该反应的离子方程式: 。
18(8分).如下图,甲、乙、丙分别表示在不同条件下可逆反应
A(g)+B(g)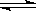 x C(g) 的生成物C在反应混合物中的百分含量(C%)和反应时间(t)的关系。
x C(g) 的生成物C在反应混合物中的百分含量(C%)和反应时间(t)的关系。
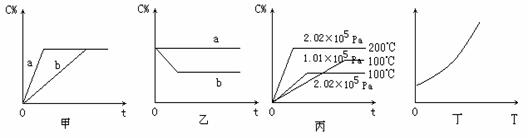

(1)若甲图中两条曲线分别表示有催化剂和无催化剂的情况,则 曲线表示无催化剂时的情况,原因是 ;
(2)若乙图表示反应达到平衡后分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入He气后的情况,则 表示恒温恒容的情况,原因是
;
(3)根据丙图可以判断该可逆反应的正反应是 热反应,计量数x的值 ;
(4)丁图表示在某固定容积的密闭容器中上述可逆反应达到平衡后某物理量随着温度(T)的变化情况,根据你的理解,丁图的纵坐标可以是 ,原因为
。
|
座号 |
|
19(6分).
(1)常温下,0.1mol·L-1的醋酸和0.1mol·L-1的盐酸各100mL分别与足量的锌粒反应,产生的气体前者比后者
(2)常温下,0.1mol·L-1的醋酸和PH=1的醋酸各100mL分别与足量的锌粒反应,产生的气体前者比后者
(3)在25℃条件下将pH=5的氯化铵溶液稀释100倍,稀释后溶液的pH为(填序号字母,下同)______。 A.5 B.7 C.3~5之间 D.5~7之间
(4)25℃时,向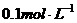 的醋酸溶液中加入少量醋酸钠晶体,当晶体溶解后测得溶液pH将 。 A、增大 B、减小 C、不变 D、无法确定
的醋酸溶液中加入少量醋酸钠晶体,当晶体溶解后测得溶液pH将 。 A、增大 B、减小 C、不变 D、无法确定
(5)室温下,向0.1mol·L-1的H2SO4中加入足量的锌粒,若想减慢制取H2的速率,但又不影响H2的体积,可以向硫酸溶液中加入 试剂
A、碳酸钠晶体 B、醋酸钠晶体 C、滴加少量硫酸铜溶液 D、水
20(10分).甲、乙、丙是前18号元素形成的常见单质,A、B、C、D是前18号元素形成的不同化合物,甲、乙、丙和A、B、C、D有如下图所示的转化关系,丙是生命活动须臾不可缺少的气态单质,请回答下列问题:
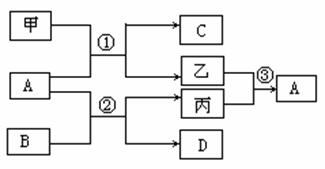
(1)若甲为金属单质,A常温下为气体,则A的化学式为 ,写出反应①的化学方程式: ;
标出反应②电子转移的方向和数目:
。
(2)若甲为非金属单质,A常温下为液态,则A的电子式为 , C的化学式为 ,
指出B的一种用途 ,写出反应②的离子方程式:
21(15分).用如图1所示装置进行相关实验(夹持仪器省略),回答下列问题:
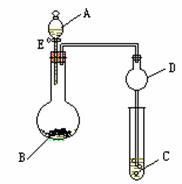
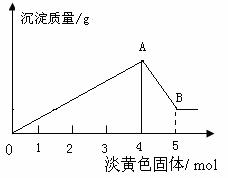
图1 图2
(1)图1中D装置在实验中的作用是 ,实验前检查该装置气
密性的方法是 ;
(2)如图1,将液体A逐滴加入到固体B中即产生气体,该气体可以是(填化学式,少于3种不得分) ;
(3)如图1,若A为浓盐酸,B为MnO2,C容器中盛KI淀粉溶液,旋开E后,给烧瓶加热,一段时间后C中的现象是 ,写出烧瓶中发生反应的化学方程式 ;
(4)如图1,溶液A中可能含有Mg2+ 、Cu2+ 、Al3+ 、Fe 3+四种阳离子,B为淡黄色固体,旋开E后,有气体放出和白色沉淀产生,淡黄色固体的物质的量与产生沉淀的物质的量的关系如图2所示,则溶液中含有的阳离子有 ; 写出 图中曲线A-B 段反应的离子方程式 ;求A溶液中存在的阳离子的物质的量浓度之比,并写出计算过程。
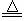 CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O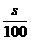 )a C、
)a C、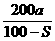 D、(1+
D、(1+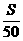 )a
)a