18.(11分)
A、B、C、D为原子序数依次增大的四种短周期元素,A、D同主族,B、C同周期。它们中的两种元素可形成多种原子个数比为1:1的化合物,甲、乙、丙、丁为其中的四种,它们的元素组成如下表:
|
化合物 |
甲 |
乙 |
丙 |
丁 |
|
元素种类 |
A、B |
A、C |
A、D |
C、D |
通常情况下,甲为气体,密度比空气小;乙为液体;丙和丁为固体且均为离子化合物。请填写下列空白:
(1)乙的电子式为 ,丁中阴离子与阳离子的个数比为
(2)已知甲是同系列中最简单的化合物,且在标准状况下,5.6 L的甲完全燃烧放出的热量为325 kJ,试写出甲的燃烧热的热化学方程式
(3)研究表明,乙是一种二元弱酸,请写出乙在水中的电离方程式
(4)已知丙的晶体结构与NaC!相似,则该晶体中与D离子距离最近的D离子有 个;有资料显示,丙是一种危险物质,其反应活性很高,在潮湿的空气中能自燃。试写出相应的化学方程式
(5)A、B、C、D所对应元素的原子半径大小顺序为 (用元素符号表示)。
 +5Cu2 S+44H
+5Cu2 S+44H ====10Cu
====10Cu +5SO2+8Mn
+5SO2+8Mn
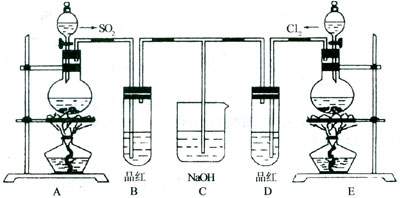
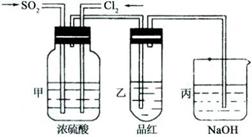
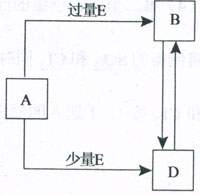 (4)某同学计划检验A中的阳离子,他还需要哪些仪器和药品:
(4)某同学计划检验A中的阳离子,他还需要哪些仪器和药品:
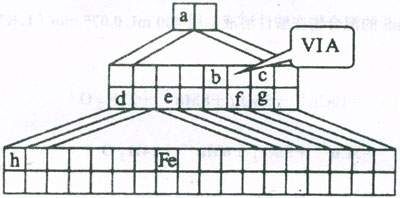
 、SO
、SO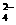
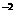 mol·L
mol·L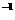 的溶液:Ba
的溶液:Ba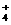 、SO
、SO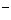 、NO
、NO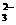
 Si+2CO↑制得粗硅
Si+2CO↑制得粗硅