1.(16分)早在几百年前,人们就发现了沼泽里的沼气,但是将沼气作为能源来利用,则是近几十年的事,随着世界性能源危机和环境污染问题的突出,利用甲烷菌在密闭的条件下分解各种有机物产生沼气,已经成为获得新能源和保护环境的重要手段之一。沼气的主要成分是CH4,还有少量CO2、H2S等。
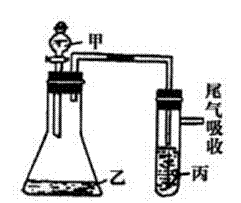
下面是某课外活动小组在实验室模拟沼气发酵制取沼气,收集较纯净甲烷并测定产生甲烷体积的实验:
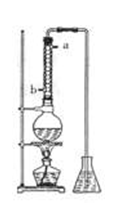
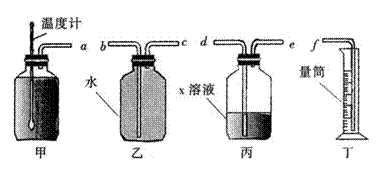 图中甲瓶是产生沼气的发酵瓶,将堆沤过的牛、马粪按比例均匀拌入沼气菌种,放进发酵瓶甲内,并加满水;乙瓶中充满水;丙瓶内盛有X溶液;丁为量筒。
图中甲瓶是产生沼气的发酵瓶,将堆沤过的牛、马粪按比例均匀拌入沼气菌种,放进发酵瓶甲内,并加满水;乙瓶中充满水;丙瓶内盛有X溶液;丁为量筒。
(1)(2分)按实验要求,将四个装置a-f各个导管口连接起来,其正确的顺序是:(填接口序号)a→ → → → →f
(2)(2分)丙瓶内盛有的X溶液为(填序号)
A.浓氨水 B.NaOH溶液 C.CuSO4溶液 D.NaCl溶液
(3)(6分)已知1000mL(标准状况)甲烷完全燃烧生成二氧化碳和液态水,放出39.75 kJ的热量,则1 mol甲烷完全燃烧生成二氧化碳和液态水所放出的能量为 。该反应的热化学方程式为 。
(4)开始实验以后,每天观察并记录,下面是其中三天的实验记录。
|
天 |
温度(℃) |
量筒内收集到的水(mL) |
|
1 |
21 |
30 |
|
2 |
14 |
16 |
|
3 |
11 |
10 |
从上述材料看,影响发酵瓶内产气量的外界因素是 ,该因素是通过影响微生物体内的 的 能力来影响产气量的。
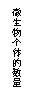
 定并验证确有NO生成,该学生设计的实验装置如下图,试回答:
定并验证确有NO生成,该学生设计的实验装置如下图,试回答:
(1)实验前要先打开A装置的活塞K1,通入一段时间氮气后再关闭K1其目的和原因
是 。
(2)装置B的作用是 。
(3)实验时A中反应停止后,打开D装置导管的活塞K2并通入氧气,若反应确有NO
产生,D中的现象是 ;实验时发
现通入氧气温度的高低对实验有较大的影响,为便于观察应通入(填“冷”或“热”)
的氧气,其原因是(用所学过的理论知识解释)
。
(4)为减小测量误差,在A中反应完成和D中出现现象后,还应进行的操作是
。
(5)若设反应中硝酸无挥发也无分解,且溶液的体积变化忽略不计,实验已测得以下
数据:铜银合金的质量、浓硝酸的物质的量浓度及体积(过量)、E装置反应生成
物中氮元素的质量;为确定合金中铜的质量分数,还需测定的数据是
(6)若实验只测定Cu的质量分数,不检验NO的产生,则在铜银合金与浓硝酸反应后,
只需简单实验操作(不使用B~E连续装置)就可达目的,简述实验过程
5.(15分)
(1)写出CO2和Na2O2反应的化学方程式:
。
(2)某学生判断SO2和Na2O2反应能生成硫酸钠,你认为他的判断合理吗?
;简要说明理由:
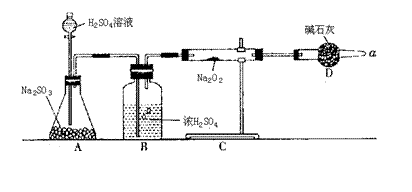 (3)该同学无法断定反应中是否有氧气生成,拟使用下列装置进行实验。
(3)该同学无法断定反应中是否有氧气生成,拟使用下列装置进行实验。
装置中B的作用是: ;
D的作用是:
(4)为确认反应产物,请完成下列实验表格
|
操
作 |
现象及结论 |
|
①确认是否有氧气生成: |
|
|
②确认是否有硫酸钠生成: |
|
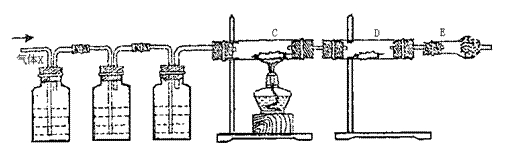
5.(18分)利用下图装置,选用适当试剂可完成实验A、B、C,并得出相应实验结论。实
 验所选用的试剂或所得结论列于下表中。
验所选用的试剂或所得结论列于下表中。
|
实验 |
所用试剂 |
实验结论 |
||
|
甲 |
乙 |
丙 |
||
|
A |
① |
高锰酸钾 |
② |
氧化性:KMnO4>Cl2>Br2 |
|
B |
盐酸 |
石灰石 |
苯酚钠溶液 |
③ |
|
C |
④ |
⑤ |
⑥ |
SO2具有漂白性 |
(1)请将表中③-⑥应填写的内容填在下面空格中
①浓盐酸 ②溴化钠溶液 ③ ④ ⑤ ⑥
(2)请利用此装置另设计一个有机实验。填写甲、乙丙中的试剂、丙中现象及由此得出
的结论。
试剂:甲 ,乙 ,丙 。
丙中观察到的现象: 。
由此实验得出的结论: 。
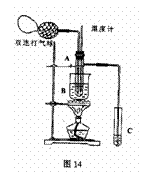
4.(18分)乙醛在催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图14所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下:
 物质 物质 |
乙醛 |
乙酸 |
甘油 |
乙二醇 |
水 |
|
沸点 |
20.8℃ |
117.9℃ |
290℃ |
197.2℃ |
100℃ |
请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为
(注明反应条件) ;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的
位置,在实验开始时温度计水银球的位置应在
;当试管A内的主要反应完成后温度计
水银球的位置应在 ,目的是
;
(3)烧杯B的作用是 ;
烧杯B内盛装的液体可以是 (写出一种即可);
(4)若想检验试管C中是否含有产物乙酸,请你在所提供的药品中进行选择,设计一个简便的实验方案。
所提供的药品中:pH试纸、红色的石蕊试纸、白色的醋酸铅试纸、碳酸氢钠粉末。实验仪器任选。
该方案为
。
3.(16分)一支干燥的小试管中装有少量白色物质(约占试管容积的1/10)。已知该白色物质是碳酸氢铵、碳酸氢钠、碳酸和氯化钠中的一种,现通过加热试管中的固体,只用蒸馏水、石蕊试纸或pH试纸进行鉴定。
(1)按照顺序写出主要实验步骤及操作要点(使用酒精灯和试管夹的方法不必叙述,其它要点要说清楚)
①
②
(2)填写下表:
|
白色物质 |
判断依据 |
有关化学方程式(或离子方程式) |
|
碳酸氢铵 |
|
|
|
碳酸氢钠 |
|
|
|
碳酸钠 |
|
|
|
氯化钠 |
|
|
 (20分)某课外活动小组的同学,在实验室做锌与浓硫酸反应实验时,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证甲、乙两位同学的判断是否正确,丙同学设计了如下图所示的实验装置(锌与浓硫酸共热时产生的气体为X,而该装置略去):
(20分)某课外活动小组的同学,在实验室做锌与浓硫酸反应实验时,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证甲、乙两位同学的判断是否正确,丙同学设计了如下图所示的实验装置(锌与浓硫酸共热时产生的气体为X,而该装置略去):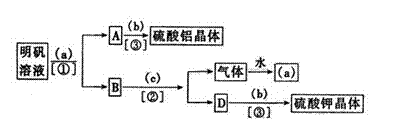 (19分)Ⅰ.(6分)下图所示:是用明矾[KAl(SO4)2·12H2O]制取硫酸铝和硫酸钾的操作步骤流程图(图中略去了沉淀物的洗涤操作),请在图中括圆号内填入适当的试剂名称,在方括号内填入适当的分离方法,并回答有关问题。
(19分)Ⅰ.(6分)下图所示:是用明矾[KAl(SO4)2·12H2O]制取硫酸铝和硫酸钾的操作步骤流程图(图中略去了沉淀物的洗涤操作),请在图中括圆号内填入适当的试剂名称,在方括号内填入适当的分离方法,并回答有关问题。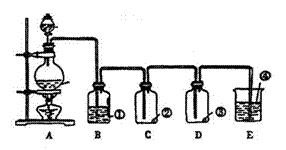 Ⅱ.(13分)某同学为了验证氯气是否有漂白性,设计了如下装置进行实验。其中①为饱和食盐水 ②为干燥的红纸 ③为浸湿的红纸 ④为氢氧化钠溶液
Ⅱ.(13分)某同学为了验证氯气是否有漂白性,设计了如下装置进行实验。其中①为饱和食盐水 ②为干燥的红纸 ③为浸湿的红纸 ④为氢氧化钠溶液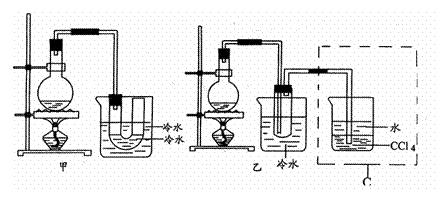
 (C2H4O)n
n C2H4O;
(C2H4O)n
n C2H4O;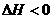
 (3)当n=3时,试写出(C2H4O)n的结构简式
。
(3)当n=3时,试写出(C2H4O)n的结构简式
。