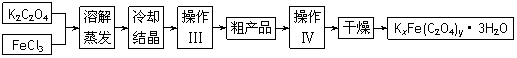
14.在1 L的密闭容器中充入1
molA(g)和1 mol B(g),于T℃时进行如下反应:A(g)+B(g) C(g)+D(g) △H<0达到平衡时,A转化了50%。在T℃时,将1
molA(g)和4 molB(g)充入同样的容器中,记录0-8
min内容器中各物质的
C(g)+D(g) △H<0达到平衡时,A转化了50%。在T℃时,将1
molA(g)和4 molB(g)充入同样的容器中,记录0-8
min内容器中各物质的
量如右表。t min时为改变条件后达平衡时所测得的数据。下列说法正确的是( )
|
时间/min |
0 |
4 |
6 |
8 |
t |
|
n[A(g)]/mol |
l |
0.25 |
nl |
nl |
0.15 |
|
n[B(g)]/mol |
4 |
3.25 |
n2 |
n2 |
3.15 |
|
n[C(g)]/mol |
0 |
0.75 |
n3 |
n3 |
0.85 |
|
n[D(g)]/mol |
0 |
0.75 |
n4 |
n4 |
0.85 |
A.反应在第4 min时处于化学平衡状态
B.前4 min,用A(g)表示的化学反应速率为0.0625 mol·L-1·min-1
C.8 min时,混合气体中C(g)的体积分数为16%
D.t min时,反应所处的温度低于T℃
非选择题
13.25℃时,几种弱酸的电离常数如下:
|
弱酸化学式 |
CH3COOH |
HCN |
H2S |
|
电离常数(25℃) |
1.8×10-5 |
4.9×10-10 |
K1=
1.3×10-7、K2=
7.1×10-15 |
25℃时,下列说法正确的是 ( )
A.等物质的量浓度的各溶液pH关系为:pH(CH3COONa)>pH(Na2S)>pH(NaCN)
B.HCN与NaOH两溶液等体积混合后若c(Na+)> c(CN-),则一定是前者的较浓
C.NaHS和Na2S混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-)
D.某浓度HCN的水溶液pH=d,则其中c(OH-)=10-d mol/L
10.下图Ⅰ、Ⅱ分别是甲、乙两同学将反应“AsO43-+2I-+2H+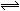 AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙向图ⅡB烧杯中逐滴加入适量40%NaOH溶液。下列叙述中正确的是 ( )
AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙向图ⅡB烧杯中逐滴加入适量40%NaOH溶液。下列叙述中正确的是 ( )

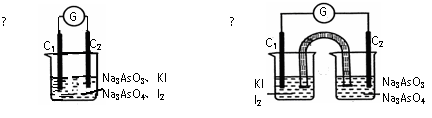
|
|
A.甲操作时,溶液颜色变浅
B.甲操作时,微安表(G)指针发生偏转
C.乙操作时,C2做正极
D.乙操作时,C1上发生的电极反应为I2+2e-=2I-
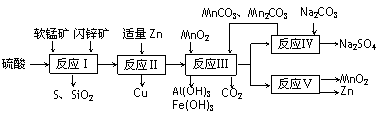 (10分)某地有软锰矿和闪锌矿两座矿山,它们的组成如下:软锰矿:MnO2含量≥65%,SiO2含量约20%,Al2O3含量约4%;闪锌矿:ZnS含量≥80%,FeS、CuS、SiO2含量约7%。科研人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如下图所示。
(10分)某地有软锰矿和闪锌矿两座矿山,它们的组成如下:软锰矿:MnO2含量≥65%,SiO2含量约20%,Al2O3含量约4%;闪锌矿:ZnS含量≥80%,FeS、CuS、SiO2含量约7%。科研人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如下图所示。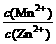 = 。
= 。