22.(11分)
I.实验室有一瓶失去标签的某白色固体,已知其成份可能是碳酸或亚硫酸的钠盐或钾盐,
且其成分单一。现某化学小组通过如下步骤来确定其成分:
(1)阳离子的确定:
实验方法及现象:
结论:此白色固体是钠盐。
(2)阴离子的确定:
①取少量白色固体于试管中,然后向试管中加入稀盐酸,白色固体全部溶解,产生
无色气体,此气体能使溴水褪色。
②要进一步确定其成分需补做如下实验:取适量白色固体配成溶液,取少许溶液于试管中,加入BaCl2溶液,出现白色沉淀。
II.确认其成分后,,由于某些原因,此白固体部分被空气氧化,该化学小组想用已知
浓度的酸性KMnO4溶液来确定变质固体中X的含量,具体步骤如下:
步骤I 称取样品1.000g。
步骤II 将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀。
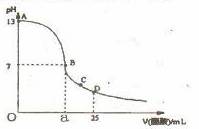
步骤III 移取25.00mL样品溶液于250mL锥形瓶中,用0.01mol·L-1KMnO4标准溶液
滴定至终点。
按上述操作方法再重复2次。
(1)写出步骤III所发生反应的离子方程式 。
(2)在配制0.01mol·L-1KMnO4溶液时若仰视定容,则最终测得变质固体中X的含量
(填“偏大”、“偏小”或“无影响”)
(3)滴定结果如下表所示:
|
滴定次数 |
待测溶液的体积 /mL |
标准溶液的体积 |
|
|
滴定前刻度/mL |
滴定后刻度/mL |
||
|
1 |
25.00 |
1.02 |
21.03 |
|
2 |
25.00 |
2.00 |
21.99 |
|
3 |
25.00 |
2.20 |
20.20 |
则该变质固体中X的质量分数为 。
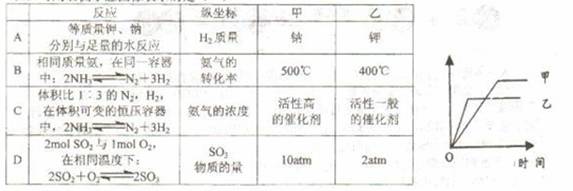
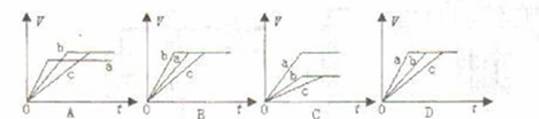
16.等质量的三份锌a、b和c,分别加入足量的稀H2SO4中,a中同时加入选题CuSO4溶液,c中加入适量CH3COONa。下列各图中表示其产生氢气总体积(V)与时间(t)的关系,其中正确的是 ( )
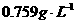 ,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族。均含D元素的乙(金属阳离子)、丙、丁微粒间的转化全为非氧化还原反应:均含F元素的乙(单质)、丙、丁微粒间的转化全为氧化还原反应。
,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族。均含D元素的乙(金属阳离子)、丙、丁微粒间的转化全为非氧化还原反应:均含F元素的乙(单质)、丙、丁微粒间的转化全为氧化还原反应。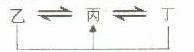
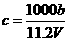 B.
B.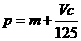 C.
C.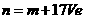 D.
D.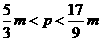
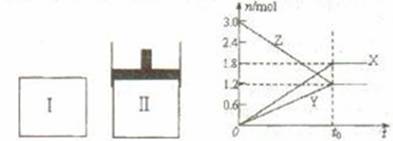
 A.该反应的化学方程式为:3X+2Y 2Z
A.该反应的化学方程式为:3X+2Y 2Z