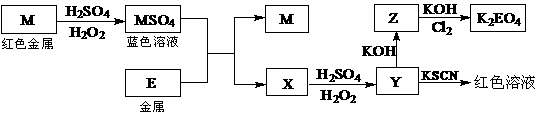
23.某中学社会实践活动小组利用假期对当地钢铁厂进行了调研,对从矿石开始到钢铁产出的工艺流程有了全面的感性认识,并对感兴趣的问题进行探讨。取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224mL(标准状况)。
(1)计算此钢样粉末中铁和碳的物质的量之比。
(2)再取三份不同质量的钢样粉末分别加到100mL相同浓度的稀H2SO4溶液中,充分反应后,测得的实验数据如下表所示:
|
实验序号 |
Ⅰ |
Ⅱ |
Ⅲ |
|
加入钢样粉末的质量/g |
2.812 |
5.624 |
8.436 |
|
生成气体的体积/L(标准状况) |
1.120 |
2.240 |
2.800 |
计算硫酸溶液的物质的量浓度。
21.有含CaO杂质的CaC2试样。某研究性学习小组的同学拟用以下三种方案测定CaC2试样的纯度。请填写下列空白:
(1)第一种方案:根据试样和水在锥形瓶中反应前后质量的变化,测定CaC2的质量分数。先称取试样1.60g,锥形瓶和水的质量为195.00g,再将试样加入锥形瓶中,反应过程中每隔相同时间测得的数据如下表:
|
|
读数次数 |
质量/g |
|
|
第1次 |
196.30 |
|
第2次 |
196.15 |
|
|
锥形瓶十水十试样 |
第3次 |
196.05 |
|
|
第4次 |
196.00 |
|
第5次 |
196.00 |
计算CaC2的质量分数时,必需用的数据是_____________________。不必作第6次读数的原因是____________________________________________。
(2)第二种方案:请从下图中选用适当的装置,设计一个实验,测定CaC2试样的纯度。
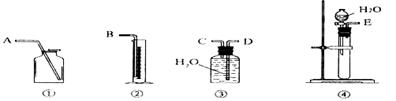
①所选用装置的连接顺序应是(填各接口的字母):_____________________________。
②若实验时称取的试样为1.40g,产生乙炔在标准状况下体积为448mL,此试样中CaC2质量分数为__________。
(3)第三种方案:称取一定质量的试样(1.60g),操作流程如下:

①操作Ⅱ的名称是________________________。
②在转移溶液时,如溶液转移不完全,则CaC2质量分数的测定结果________(填“偏大”、“偏小”或“不变”)。
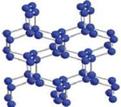 (2)E的外围电子排布式为 ,A与D形成的一种化合物是一种常见的消毒剂,其结构式为
,分子中含有的化学键有
(离子键、极性键、非极性键)。
(2)E的外围电子排布式为 ,A与D形成的一种化合物是一种常见的消毒剂,其结构式为
,分子中含有的化学键有
(离子键、极性键、非极性键)。