14.在反应3BrF3+5H2O=HB rO3+Br2+9HF+O2↑中,若有5molH2O参加反应,则被水还原的BrF3的物质的量为 ( )
A.3mol B.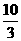 mol C.
mol C. mol D.2 mol
mol D.2 mol
14.在反应3BrF3+5H2O=HB rO3+Br2+9HF+O2↑中,若有5molH2O参加反应,则被水还原的BrF3的物质的量为 ( )
A.3mol B.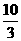 mol C.
mol C. mol D.2 mol
mol D.2 mol