17.(12分)下表列出了部分常见含有10电子和18电子的粒子,回答下列问题。
|
10电子粒子 |
CH4、NH3、H2O、HF、Na+、Al3+、NH4 +、F- |
|
18电子粒子 |
H2S、HCl、K+
、S2- 、HS﹣、Cl- |
(1)其中空间构型为正四面体的分子的是 ;受热最难分解的分子是 。
(2)其中能与OH-反应的分子有 ;
既能与H+反应又能与OH﹣反应的粒子有 。
(3)写出一种由表中粒子组成的离子化合物水溶液呈酸性的离子方程式
。
(4)由第二周期元素形成的氢化物A和B都含有18电子, A是一种6原子分子,可做火箭发动机的燃料,B是一种常见强氧化剂。已知16g液态A与液态B充分反应生成一种液态10电子分子和一种气态单质,并放出838 kJ热量。写出A与B反应的热化学方程式

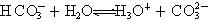
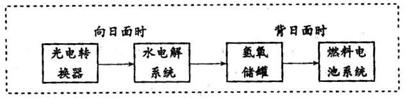 下图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法不正确的是
下图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法不正确的是
 4NO
(g)+ 6H2O(g) ΔH=akJ/mol
4NO
(g)+ 6H2O(g) ΔH=akJ/mol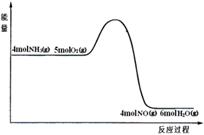 反应过程中能量变化如图所示
反应过程中能量变化如图所示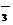 +OH-== CO
+OH-== CO +H2O
+H2O