18、有四种钠盐溶液A、B、C、D,其酸根均可用RO3n-表示(n≤2,其中R为短周期元素,且原子序数依A→D递增),现将它们取适量两两混合,并用足量硫酸酸化,其中两组实验现象如下:
|
组别 |
混合液 |
现象 |
|
I |
A、C |
白色沉淀和无色气体 |
|
II |
B、D |
无色气体 |
且知实验后I、II组所得溶液中均只含有同一种钠盐
(1)写出各酸根离子的符号A______B________C_____________D________
(2)写出两组实验中发生反应的离子方程式
I.
II.
15、类比是化学学习中常用的方法之一,已知硝酸能把铁氧化为硝酸铁,但当铁过量时,产物是硝酸亚铁。某同学受此启发,提出一个相似的观点:氯气与铁粉反应,当氯气足量时生成氯化铁,当铁粉过量时产物是氯化亚铁。为判断该观点是否正确,该同学将一根细的纯铁丝分别在足量和少量的氯气中点燃,取其表面生成物并分别编号为A、B,然后通过实验确定其成分。探究过程如下:
(1)提出假设:A是氯化铁,B是氯化亚铁
(2)设计实验方案,分别取A、B的溶液进行以下实验,但实验现象相同。请填写下表中的空格。
|
实验方法 |
实验现象 |
结论 |
|
分别向A、B溶液中加入硫氰化钾溶液 |
|
固体物质中有氯化铁 |
|
分别向高锰酸钾溶液中加入适量A、B溶液 |
高锰酸钾溶液颜色均无明显变化 |
固体物质中不含 ____ |
(3)根据上述实验结论,写出氯气与铁粉加热时发生反应的化学方程式 ____________________
(4)为进一步探究氯化铁溶液的性质,他又用A溶液做了如下一些实验,其中明显错误的是__________
A、将A溶液沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔现象
B、向A溶液中加入少量铁粉,铁粉溶解,溶液颜色加深
C、在A溶液中滴加氢氧化钠浓溶液,出现红褐色沉淀
D、将A溶液加热蒸干并灼烧,得到氯化铁固体
(5)实际应用:氯化铁溶液作印刷电路板腐蚀剂,腐蚀后的废液中含有氯化铁、氯化亚铁、氯化铜,某研究性学习小组的同学们设计了两种从废液中回收铜的方案:
方案1:向废液中加入过量的铁粉,充分反应后,过滤。在所得滤渣中加入足量的盐酸,充分反应后,再过滤即得铜。方案1中涉及的四种阳离子的氧化性由强到弱的顺序为 _____________
方案2:在废液中加入适量的盐酸调节溶液的PH=1,用铜和石墨作电极进行电解。当观察到阴极上有少量气泡产生时,即停止电解,这时要回收的铜已全部析出。方案2中铜作________极,所发生的电极反应为 _____________________ (若有多个电极反应,请按照反应发生的先后顺序全部写出)
方案2在电极上直接回收铜,操作上比方案1简便,但方案2也有不足之处,主要为_________________
14、现有部分短周期元素的性质或原子结构如下表:
|
元素代号 |
元素性质或原子结构 |
|
T |
M层上的电子数为6个 |
|
X |
最外层电子数是次外层电子数的2倍 |
|
Y |
常温下单质为双原子分子,其氢化物水溶液呈碱性 |
|
Z |
元素最高正价是+7 |
下列叙述正确的是
A、元素X的一种同位素可测定文物年代,这种同位素的符号是12C
B、元素Z的非金属性比元素T弱
C、Y和T位于同一主族
D、T、X、Y、Z四种元素的最高价氧化物水化物中化学性质明显不同于其它三种的是碳酸
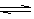 2C(g) ;△H=-QkJ/mol(Q>0).有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为Q1kJ;在相同条件下,向乙容器中加入2molC达到平衡后吸收热量为Q2kJ,已知Q1=3Q2。下列叙述正确的是
2C(g) ;△H=-QkJ/mol(Q>0).有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molA和3molB,在一定条件下达到平衡时放出热量为Q1kJ;在相同条件下,向乙容器中加入2molC达到平衡后吸收热量为Q2kJ,已知Q1=3Q2。下列叙述正确的是