摘要:可逆反应A2C(g) ;△H=-QkJ/mol.有甲.乙两个容积相同且不变的密闭容器.向甲容器中加入1molA和3molB.在一定条件下达到平衡时放出热量为Q1kJ;在相同条件下.向乙容器中加入2molC达到平衡后吸收热量为Q2kJ.已知Q1=3Q2.下列叙述正确的是 A.甲中反应达到平衡时.Q1=Q B.达到平衡时.甲中C的体积分数比乙大 C.达到平衡后.再向乙中加入0.25molA.0.75molB.1.5molC,平衡向生成C的方向移动 D.乙中的热化学反应方程式为2C(g) A; △H=+Q2kJ/mol
网址:http://m.1010jiajiao.com/timu3_id_373403[举报]
下图为可逆反应A(g)+2B(g)nC(g) △H>0生成物C的浓度随压强变化并建立平衡的关系图,则n值与压强p1、p2的关系正确的是 ( )
A. p2>p1,n<3
B. p2>p1,n>3
C. p1>p2,n<3
D. p1>p2,n>3
查看习题详情和答案>>
在一定条件下,对于密闭容器中进行的可逆反应A(g)+3B(g)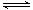
|
A.A、B、C的分子数之比为1∶3∶2
B.A、B、C的浓度相等
C.单位时间生成 n mol A,同时生成 3n mol B
D.生成C的速率与C分解的速率相等
查看习题详情和答案>>
(12分)有可逆反应A(g)+B(g) xC(g)+D(g),某温度时,在固定容积为2L的密闭容器内充入一定量的A、B,并保持温度不变。A、B、C、D物质的量随时间的变化如图所示:
(1)根据图中所示,x=_______________;该反应的平衡状态为图中的____________min;
(2)0~5min的平均反应速率v(A)=_______________________________(用小数表示)。
(3)6min时改变影响平衡的一个条件,A、B、C、D的变化曲线如图中6~8min所示,则平衡_________移动(填“向左”、“向右”或“不”),可能的原因是________(选填序号)。
a、增大A的物质的量 b、加入催化剂
c、增加C的物质的量 d、减小容器体积
(4)若反应一开始就加入了合适的催化剂,在图中画出气体A在0~6min时的变化曲线。
查看习题详情和答案>>
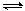
 nC(g)
(正反应放热)生成物C的浓度随压强变化并建立平衡的关系图,则n值与压强P1、P2的关系正确的是
nC(g)
(正反应放热)生成物C的浓度随压强变化并建立平衡的关系图,则n值与压强P1、P2的关系正确的是
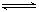 2C(g)达到平衡状态的标志是
2C(g)达到平衡状态的标志是