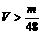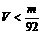9、(17分)下表是元素周期表的一部分,表中所列字母分别代表化学元素。就表中所列字母所代表的元素,回答下列问题。
|
a |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
b |
c |
|
|
|
|
d |
|
|
|
|
|
|
|
|
|
|
e |
f |
g |
|
h |
|
|
|
|
|
|
|
|
|
i |
|
|
|
|
|
|
|
|
|
|
请填空:
(1)元素电负性的X数值表示不同的原子在分子内吸引电子能力的大小,若X值越大,其原子吸引电子能力越强,在所形成的分子中成为带负电荷的一方。当两种元素的电负性差值越大,键的极性越大。小于1.7时,这两种元素通常形成共价化合物。下表是部分主族元素的电负性:
|
H:2.1 |
|
|
|
|
|
|
|
Li:1.0 |
Be:1.5 |
B:2.0 |
C:2.5 |
N:3.0 |
O:3.5 |
F:4.0 |
|
Na:0.9 |
Mg:y |
Al:1.5 |
Si:1.8 |
P:2.1 |
S:2.5 |
Cl:3.0 |
|
K:0.8 |
Ca:1.0 |
Ga:1.6 |
Ge:1.8 |
As:2.0 |
Se:2.4 |
Br:2.8 |
①X值的大小也可以作为判断金属性和非金属性的强弱的尺度。金属的X值一般小于 。d元素的电负性(y)的大小范围为 。由上表可以得出同周期元素的电负性X值与原子半径大小的一般关系是: 。
②在元素周期表中X值最大的元素,与a元素形成的化合物不能保存在玻璃容器中,原因是(用化学方程式表示) 。
(2)元素c与h形成的化合物是一种广谱型的消毒剂,根据世界环保联盟的要求,此化合物将逐步取代Cl2成为自来水的消毒剂,此化合物的化学式为: ,它的晶体类型是: 。
(3)a元素和b元素组成的化合物的空间构型是 (不用画图),工业上合成此化合物的适宜条件是 。
(4)e与h形成的化合物水解的离子方程式为 。
(5)i元素在元素周期表中的位置是 。
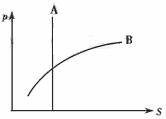 已知摩尔质量相等的化合物A和B,在25℃时,其溶解度(S)与压强(P)的关系如图所示,则在该温度下,同体积的A和B溶于等体积水(均形成溶液)后,c(A)与c(B)关系正确的是( )
已知摩尔质量相等的化合物A和B,在25℃时,其溶解度(S)与压强(P)的关系如图所示,则在该温度下,同体积的A和B溶于等体积水(均形成溶液)后,c(A)与c(B)关系正确的是( )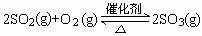 一定温度下,在容积可变的容器中,反应达到平衡时,SO2(g)、O2(g)和SO3(g)的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,按下列要求改变条件,达到新平衡时各物质的百分含量与原平衡相同的是( )
一定温度下,在容积可变的容器中,反应达到平衡时,SO2(g)、O2(g)和SO3(g)的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,按下列要求改变条件,达到新平衡时各物质的百分含量与原平衡相同的是( ) 2MoO3 + 4SO2;
2MoO3 + 4SO2; MoO3 + H2O;⑤用还原剂将MoO3还原成金属钼。
MoO3 + H2O;⑤用还原剂将MoO3还原成金属钼。
 (14分)(1)①
②
③
④
(14分)(1)①
②
③
④