(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较
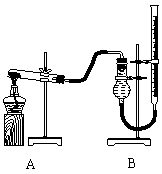 用右图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
用右图装置进行实验,实验时均以生成25 mL气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
|
实验序号 |
KClO3质量 |
其它物质质量 |
待测数据 |
|
④ |
1.2 g |
无其他物质 |
|
|
⑤ |
1.2 g |
CuO 0.5 g |
|
|
⑥ |
1.2 g |
MnO2 0.5 g |
|
回答下列问题:
⑶上述实验中的“待测数据”指_____________;
⑷本实验装置图中量气装置B由干燥管、乳胶管和50 mL滴定管改造后组装而成,此处所用滴定管是___________(填“酸式”或“碱式”)滴定管;
⑸若要证明实验⑤中干燥管内收集的气体是O2,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞
____________________________________________________;
⑹为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a._______________________________,b.CuO的化学性质有没有改变。
21、(10分)实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:
(1)配制100mL 0.10mol/L NaOH标准溶液。
①主要操作步骤:计算→称量→溶解→(冷却后) →洗涤→ 定容→
→将配制好的溶液倒入试剂瓶中,贴上标签。
②称量0.4克氢氧化钠固体所需仪器有:天平(带砝码、镊子)、烧杯、 。
(2)取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2-3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作2-3次,记录数据如下。
|
实验编号 |
NaOH溶液的浓度 (mol/L) |
滴定完成时,NaOH溶液滴入的体积(mL) |
待测盐酸溶液的体积 (mL) |
|
1 |
0.10 |
22.62 |
20.00 |
|
2 |
0.10 |
22.72 |
20.00 |
|
3 |
0.10 |
22.80 |
20.00 |


 ①排除碱式滴定管中气泡的方法应
①排除碱式滴定管中气泡的方法应
采用操作 ,(填图编号)
轻轻挤压玻璃球使尖嘴部分充满碱液。
甲 乙 丙
②滴定达到终点的标志是 。
③根据上述数据,可计算出该盐酸的浓度约为 (保留两位小数)
④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有 。
A、滴定终点读数时俯视读数
B、酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C、锥形瓶水洗后未干燥 D、称量前NaOH固体中混有Na2CO3固体
E、配制好的NaOH标准溶液保存不当,部分与空气中的CO2反应生成了Na2CO3
F、碱式滴定管尖嘴部分有气泡,滴定后消失
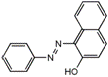 A.该物质的分子式为C16H12N2O;
A.该物质的分子式为C16H12N2O;  ==Al(OH)3↓+HCO
==Al(OH)3↓+HCO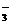
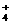 +HSO
+HSO +NH3↑+2H2O
+NH3↑+2H2O xC(g);△=?符合下图(a)所示的关系,由
xC(g);△=?符合下图(a)所示的关系,由 此推断关于图(b)的说法正确的是
此推断关于图(b)的说法正确的是