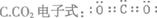0 34111 34119 34125 34129 34135 34137 34141 34147 34149 34155 34161 34165 34167 34171 34177 34179 34185 34189 34191 34195 34197 34201 34203 34205 34206 34207 34209 34210 34211 34213 34215 34219 34221 34225 34227 34231 34237 34239 34245 34249 34251 34255 34261 34267 34269 34275 34279 34281 34287 34291 34297 34305 447348
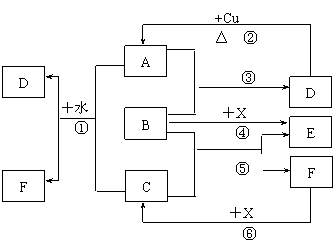 (10分)已知A-F是中学化学中常见物质,其中A、C、E、F为气体,B、D为液体,D的消费量常作为一个国家工业发达水平的一种标志,F的浓溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末,B分子中有18个电子。反应中部分生成物已略去。
(10分)已知A-F是中学化学中常见物质,其中A、C、E、F为气体,B、D为液体,D的消费量常作为一个国家工业发达水平的一种标志,F的浓溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末,B分子中有18个电子。反应中部分生成物已略去。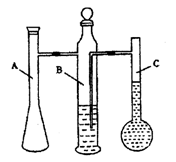 (12分)学生甲利用下图所示实验装置来测定镁元素的相对原子质量
(12分)学生甲利用下图所示实验装置来测定镁元素的相对原子质量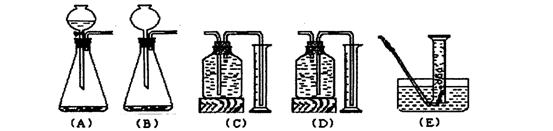 (3)学生乙利用实验室常用的仪器,也组装了一套与学生甲具有相同原理的实验装置。你认为学生乙应选用下列仪器中的________(填编号,多选扣分)
(3)学生乙利用实验室常用的仪器,也组装了一套与学生甲具有相同原理的实验装置。你认为学生乙应选用下列仪器中的________(填编号,多选扣分)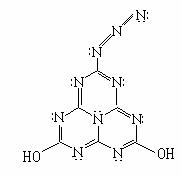 ④最后通入足量的SO2气体,请回答下列问题:
④最后通入足量的SO2气体,请回答下列问题: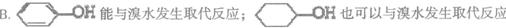
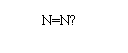 A、N2的结构式:
B、热化学方程式:H++OH-=H2O;△H=-57.3kJ/mol
A、N2的结构式:
B、热化学方程式:H++OH-=H2O;△H=-57.3kJ/mol