4、溶液的浓缩
(1)加入浓溶液
(2)加溶质
(3)蒸发蒸发溶剂(不适用于挥发性溶质,如盐酸、氨水)
[例]欲使5%的CuSO4 溶液A g变为10%的溶液,可采取下列措施:①加CuSO4 ②加CuSO4·5H2O ③加20%的CuSO4 溶液④蒸发溶剂。求上述四种情况下所需物质的质量。
☆例题精析
[例1](全国2003-14)某温度下向100g澄清的饱和石灰水中加入5.6g生石灰,充分反应后恢复到原来的温度,则下列说法正确的是( )
A 沉淀的质量为5.6g
B 沉淀物的质量为7.4g
C 饱和石灰水的质量大于98.2g
D 饱和石灰水的质量小于98.2g
[例2]已知某盐在不同温度下的溶解度如下表.若把质量分数为22%的该盐溶液,由50℃逐渐冷却,则开始析出晶体的温度范围是( )
|
温度℃ |
0 |
10 |
20 |
30 |
40 |
|
溶解度 (g/100g水) |
11.5 |
15.1 |
19.4 |
24.4 |
37.6 |
A、0℃~10℃ B 、10℃~20℃ C 、20℃~30℃ D 、30℃~40℃
[例3]已知t℃时,某物质的不饱和溶液a g中含有溶质m g。若将该溶液蒸发b g水并恢复到t℃时,析出溶质m1 g ;若将原溶液蒸发c g水并恢复到t℃时,则析出溶质m2 g。S表示该物质在t℃时的溶解度,则下列正确的是( )
A 、 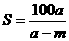 B、
B、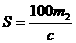
C、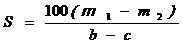 D、
D、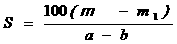
[例4]如图是几种盐的溶解度曲线,下列说法正确的是( )
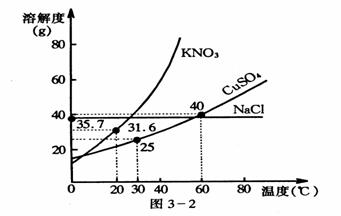
A、40℃时,将35g食盐溶于100g水中,降温至0℃时,可析出NaCl 晶体
B、20℃时,硝酸钾饱和溶液的质量分数是31.6%
C、60℃时,200g水中溶解80g硫酸铜达饱和。当降温至30℃时,可析出30g CuSO4 晶体D、30℃时,将35g KNO3 和35g NaCl 同时溶于100g水中,蒸发时,先析出的是NaCl 。
备选[例5](1998年全国)下面是四种盐在不同温度下的溶解度(g/100g水)
|
|
NaNO3 |
KNO3 |
NaCl |
KCl |
|
10℃ |
80.5 |
20.9 |
35.7 |
31.0 |
|
100℃ |
175 |
246 |
39.1 |
56.6 |
(计算时假定:①盐类共存时不影响各自的溶解度;②过滤晶体时,溶剂损耗忽略不计)
(1)取23.4g NaCl 和40.4g KNO3 ,加70.0 H2O ,加热溶解。在100℃ 时蒸发掉50.0g H2O ,维持该温度,过滤析出晶体,计算所得晶体的质量(m高温). 将滤液冷却至10℃, 待充分结晶后,过滤.计算所得晶体的质量(m 低温)。
(2)另取34g NaNO3 和29.8 KCl ,同样进行如上实验.10℃时析出的晶体是_________(写化学式).100℃和10℃得到的晶体质量(m’高温和m’低温)分别是多少?
1、溶液、胶体与浊液三类分散系的比较
|
|
浊液 悬浊液 乳浊液 |
溶 液 |
胶 体 |
|
定 义 |
固体小颗粒 小液滴悬浮悬浮于液体 于液体 |
一种或几种物质分散到另一种物质形成均一稳定混合物 |
分散质微粒直径在 10-9~10-7m之间的分散系 |
|
本质差别 |
分散质微粒直径>10-7m |
分散质微粒直径<10-9m |
分散质微粒直径在 10-9~10-7m |
|
性 质 |
不均一、不透明、不稳定,静置分层或颗粒下降 |
均一、透明、稳定, 无丁达尔现象 |
均一、透明、稳定,有丁达尔现象、布朗运动、电泳现象,可以凝聚。 |
|
能否透过滤 纸 |
悬浊液不能 |
能 |
能 |
|
能否透过半 透
膜 |
不能 |
能 |
不能 |
|
实 例 |
泥水、油水混合物 |
食盐水、碘酒 |
Fe(OH)3 胶体 |
15、(16分)
(1) , , 。
(2) 。(3) 。
|
坩埚质量 |
坩埚与晶体总质量 |
加热后坩埚与固体总质量 |
测得晶体中结晶水的个数 |
误差(偏高或偏低) |
|
11.7g |
22.7g |
18.6g |
|
|
(4)
(5)

 (2)对于升温,为保持饱和,需增加溶质的质量计算,一般可依公式:
(2)对于升温,为保持饱和,需增加溶质的质量计算,一般可依公式: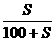 ×100%
×100%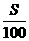 =
= 

 ×100%
×100% ①概念:分散质粒子的直径介于10-9~10-7m之间的分散系
①概念:分散质粒子的直径介于10-9~10-7m之间的分散系 液溶胶:Fe(OH)3 胶体、H4SiO4 溶胶
液溶胶:Fe(OH)3 胶体、H4SiO4 溶胶 丁达尔现象--据此可区分溶液和胶体
丁达尔现象--据此可区分溶液和胶体 金属氧化物、金属氢氧化物的胶粒带正电。
金属氧化物、金属氢氧化物的胶粒带正电。