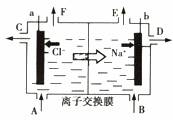
26.(16分)A、B、C、D、E、F、G都是短周期的主族元素,它们的核电荷数依次增大。元素A 的原子核内仅有一个质子,A、D同主族,B、C同周期且与A能形成相同电子数的化合物,C与F同主族,F的质子数为C的2倍,元素E 的最外层电子数比K层电子数多1,B、C、F的质子数之和等于E、G的质子数之和。请回答下列问题:
(1)写出由上述至少两种元素组成的具有漂白作用的物质的化学式______(请写出四种)。]
(2)A分别与B、F、G能形成相应的常见的三种化合物,同温同压下这三种化合物在水中的溶解度由大到小的顺序为_______________________(用化学式表示)。
(3)由A、B、C、D四种元素组成的一种常见化合物X的溶液分别与由C、D、E三种元素组成的一种化合物 Y的溶液和由E、G两种元素组成的一种化合物Z的溶液都能反应得到同一种白色沉淀,写出上述两个反应的离子方程式X+Y:_________________________;
X+Z:________________________________________。
(4)D、E两种元素的原子都能形成相应的离子,则两离子半径大小关系为_____________(用离子符号表示);将D、E两种元素的单质同时投入水中,充分反应后,测得溶液中只有一种溶质,且无固体剩余,则所投入到水中的D、E单质的质量比为_____________,上述反应总的化学方程式为________________________________。
|
已知在常温下测得浓度均为0.1 mol∙L-1下列6种溶液的pH:
|
溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
C6H5ONa |
|
pH |
8.1 |
8.8 |
11.6 |
10.3 |
11.1 |
11.3 |
(1)请根据上述信息判断下列反应能发生的是_____________(填编号)。
A.CO2+H2O+2NaClO=Na2CO3+2HClO
B.CO2+H2O+NaClO=NaHCO3+HClO
C.CO2+H2O+ C6H5ONa →NaHCO3+ C6H5OH
D.CO2+H2O+ 2C6H5ONa →Na2CO3+ 2C6H5OH
E.Na2CO3+ C6H5OH →NaHCO3+ C6H5ONa
F.CH3COOH+NaCN = CH3COONa+HCN
(2)一些复分解反应的发生还遵循其他规律。下列变化都属于复分解反应:
①将石灰乳与纯碱溶液混合可制得苛性钠溶液。
②向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打固体。
③蒸发 KCl和NaNO3的混合溶液,首先析出NaCl晶体。
根据上述反应,总结出复分解反应发生的另一规律为________________。
(3)物质的量浓度均为0.05 mol∙L-1的下列5种物质的溶液中,pH由大到小的顺序是_____________(填编号)。
①C6H5OH ②CH3COOH ③HClO4 ④HClO ⑤H2SO4
(4)一定温度下,向等体积的纯水中分别加入等物质的量的下列物质:①NaOH ②CH3COOH ③NaClO,则水的电离程度最大的是__________(填编号)。一定温度下,向等体积纯水中分别加入等物质的量的CH3COONa和NaCN,两溶液中离子的总物质的量分别为n1和n2,则它们的关系为n1_____n2(填“>”、“<”或“=”)。
 2CuO+4NO2↑+O2↑。某学生将适量的Cu(NO3)2固体放入试管中加热使其分解,用集气瓶收集产生的气体,将带火星的木条伸入集气瓶中,木条复燃。下列有关说法正确的是: ( )
2CuO+4NO2↑+O2↑。某学生将适量的Cu(NO3)2固体放入试管中加热使其分解,用集气瓶收集产生的气体,将带火星的木条伸入集气瓶中,木条复燃。下列有关说法正确的是: ( )

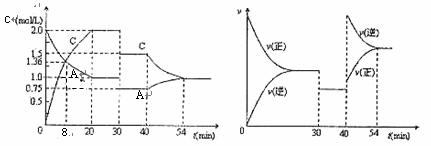
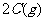 达到平衡后,只改变反应的一个条件,测得容器中物质A、C的浓度及反应速率随时间变化如下图所示。下列说法中正确的是: (
)
达到平衡后,只改变反应的一个条件,测得容器中物质A、C的浓度及反应速率随时间变化如下图所示。下列说法中正确的是: (
)
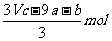
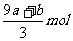 D.
D.