32.(8分)[物质结构与性质]
现有部分前四周期元素的性质或原子结构如下表:
|
元素编号 |
元素性质或原子结构 |
|
A |
第三周期中的半导体材料 |
|
B |
L层s电子数比p电子数少l |
|
C |
第三周期主族元素中其第一电离能最大 |
|
D |
前四周期元素中其未成对电子数最多 |
(1)B单质分子中,含有 个σ键和 个π键,元素B的气态氢化物的空间构型为 。
(2)C单质的熔点 A单质的熔点(填“高于”或“低于”),其原因是:
(3)写出元素D基态原子的电子排布式: 。
30.(12分)某校化学研究小组的同学已知碳酸钠和碳酸氢钠的化学性质,并对碳酸钠和碳酸氢钠的活泼性进行了如下实验探究:
I.为了鉴别碳酸钠和碳酸氢钠两种白色固体,小组成员用不同的方法进行了实验,如 下图装置所示:
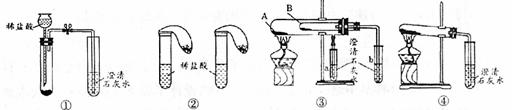
(1)只根据图①、图②所示实验,能够明确达到实验目的的是 (填“①”或“②”)
(2)若用图③所示实验装置验证碳酸钠比碳酸氢钠的稳定性好,则碳酸氢钠应装入
管中(填“A”或“B”)。
(3)有同学提出用图④所示实验装置就能在一次实验、一个反应中比较出碳酸钠和碳酸氢钠的热稳定性相对强弱,你认为这个说法 (填“正确”或“不正确”)
II.已知:10℃时,在烧杯中加入0.1mol/L的NaHCO3溶液400mL,测得该溶液在不同温度下的pH(见下表):
|
温度(℃) |
10 |
20 |
30 |
50 |
|
pH |
8.3 |
8.4 |
8.5 |
8.9 |
甲同学将200mL、20℃、0.lmol/L的NaHCO3溶液置于烧杯中加热至50℃,测其pH为8.9;再将溶液冷却至20%,测其pH仍为8.4。乙同学将200mL、20℃、0.1mol/L的NaHCO3溶液置于烧杯中加热至90%一段时间后,将溶液冷却至20℃,测其pH为10.1(溶液体积不变)。
请对上述实验现象作出说明。
[选做部分]
共8个题,考生从中选择2个物理题、1个化学题和1个生物题作答
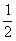 O2(g)==CO(g);⊿H=-Q1kJ·mol-1,2CO(g)+ O2(g)==2CO2(g);⊿H=-Q2kJ·mol-1,据此推断,下列说法正确的是(Q、Q均为正数,且其他条件相同) ( )
O2(g)==CO(g);⊿H=-Q1kJ·mol-1,2CO(g)+ O2(g)==2CO2(g);⊿H=-Q2kJ·mol-1,据此推断,下列说法正确的是(Q、Q均为正数,且其他条件相同) ( )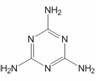 则其化学式为C3N6H6
,
则其化学式为C3N6H6
,