摘要:30.某校化学研究小组的同学已知碳酸钠和碳酸氢钠的化学性质.并对碳酸钠和碳酸氢钠的活泼性进行了如下实验探究: I.为了鉴别碳酸钠和碳酸氢钠两种白色固体.小组成员用不同的方法进行了实验.如 下图装置所示: (1)只根据图①.图②所示实验.能够明确达到实验目的的是 (2)若用图③所示实验装置验证碳酸钠比碳酸氢钠的稳定性好.则碳酸氢钠应装入 管中. (3)有同学提出用图④所示实验装置就能在一次实验.一个反应中比较出碳酸钠和碳酸氢钠的热稳定性相对强弱.你认为这个说法 II.已知:10℃时.在烧杯中加入0.1mol/L的NaHCO3溶液400mL.测得该溶液在不同温度下的pH: 温度(℃) 10 20 30 50 pH 8.3 8.4 8.5 8.9 甲同学将200mL.20℃.0.lmol/L的NaHCO3溶液置于烧杯中加热至50℃.测其pH为8.9,再将溶液冷却至20%.测其pH仍为8.4.乙同学将200mL.20℃.0.1mol/L的NaHCO3溶液置于烧杯中加热至90%一段时间后.将溶液冷却至20℃.测其pH为10.1. 请对上述实验现象作出说明. [选做部分] 共8个题.考生从中选择2个物理题.1个化学题和1个生物题作答
网址:http://m.1010jiajiao.com/timu_id_1743471[举报]
(12分)某校化学研究小组的同学已知碳酸钠和碳酸氢钠的化学性质,并对碳酸钠和碳酸氢娜的活泼性进行了如下实验探究:
I、为了鉴别碳酸钠和碳酸氢钠两种白色固体,小组成员用不同的方法进行了实验,如下图装置所示:
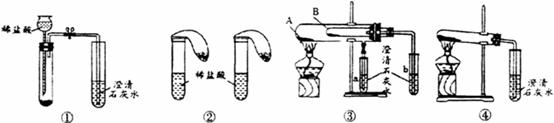
(1)只根据图①、图②所示实验,能够明确达到实验目的的是_______(填“①”或 “②”)
(2)若用图③所示实验装置验证碳酸钠比碳酸氢钠的稳定性好,则碳酸氢钠应装入_________管中(填“A”或“B”)。
(3)有同学提出用图④所示实验装置就能在一次实验、一个反应中比较出碳酸钠和碳酸氢钠的热稳定性相对强弱,你认为这个说法___________(填“正确”或“不正确”)
Ⅱ、已知:10℃时,在烧杯中加入![]() 的
的![]() 溶液400mL,测得该溶液在不同温度下的pH(见下表):
溶液400mL,测得该溶液在不同温度下的pH(见下表):
| 温度(℃) | 10 | 20 | 30 | 50 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 |
甲同学将![]() 的
的![]() 溶液置于烧杯中加热至50℃,测其pH为8.9;再将溶液冷却至20℃,测其pH仍为8.4。乙同学将200mL、20℃、
溶液置于烧杯中加热至50℃,测其pH为8.9;再将溶液冷却至20℃,测其pH仍为8.4。乙同学将200mL、20℃、
![]() 的
的![]() 溶液置于烧杯中加热至90℃一段时间后,将溶液冷却至
溶液置于烧杯中加热至90℃一段时间后,将溶液冷却至
20℃,测其pH为10.1(溶液体积不变)。
请对上述实验现象作出说明。
查看习题详情和答案>>某校化学研究性学习小组设计如下实验方案,测定放置已久的小苏打样品中纯碱的质量分数。
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。实验中加热至恒重的目的是____。
(2)方案二:按下图装置进行实验。并回答以下问题:
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。实验中加热至恒重的目的是____。
(2)方案二:按下图装置进行实验。并回答以下问题:
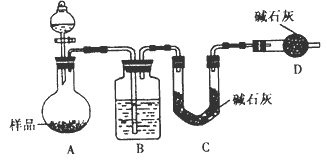
①实验前应先____。分液漏斗中应该装___(填“盐酸”或“稀硫酸”)。 D装置的作用是___;
②实验中除称量样品质量外,还需称___装置(用字母表示)前后质量的变化;
③根据此实验得到的数据,测定结果有较大误差。因为实验装置还存在一个明显缺陷,该缺陷是____。
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液,过滤洗涤,干燥沉淀,称量同体质量,计算:
①过滤操作中,除了烧杯、漏斗外还用到的玻璃仪器有___;
②实验中判断沉淀是否完全的方法是___;
③若加入试剂改为氢氧化钡,已知称得样品9. 5 g,干燥的沉淀质量为19.7 g,则 样品中碳酸钠的质量分数为___(保留一位小数)。
查看习题详情和答案>>
②实验中除称量样品质量外,还需称___装置(用字母表示)前后质量的变化;
③根据此实验得到的数据,测定结果有较大误差。因为实验装置还存在一个明显缺陷,该缺陷是____。
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液,过滤洗涤,干燥沉淀,称量同体质量,计算:
①过滤操作中,除了烧杯、漏斗外还用到的玻璃仪器有___;
②实验中判断沉淀是否完全的方法是___;
③若加入试剂改为氢氧化钡,已知称得样品9. 5 g,干燥的沉淀质量为19.7 g,则 样品中碳酸钠的质量分数为___(保留一位小数)。
I.某校化学学习小组为了探究草酸(H2C2O4)的化学性质,设计了如下实验:
小组成员在做草酸溶液与酸性高锰酸钾溶液反应实验时发现,溶液褪色先慢后快。
(1)上述H2C2O4溶液与酸性KMnO4溶液反应的离子方程为 。
(2)为了探究此反应速率由小变大的原因,甲同学做了如下实验(表中“一”表示未加入该试剂)。
甲同学由此能够得出结论:
II.乙同学查资料得知“菠菜中富含可溶性草酸盐和碳酸盐”, 决定用实验验证这一事实并检测草酸盐含量。进一步查阅资料得知,草酸(H2C2O4)是酸性强于醋酸的二元弱酸,对应的钙盐(CaC2O4)不溶于醋酸,能溶于强酸。
(1) 欲准确测定菠菜中草酸盐含量,回答有关问题:
①操作:取m g菠菜样品,将其中草酸盐转化为 CaC2O4 沉淀分离出来,用盐酸溶解后,溶液转入100mL容量瓶中加水配制成100mL溶液。每次移取25.00mL该溶液,用0.0100mol·L-1 KMnO4标准溶液滴定,滴定实验重复操作2 —3次。平均消耗标准溶液V mL。
②计算:菠菜中草酸盐(以C2O42-计)的质量分数为 。(只列式不计算,已知:C2O42-的的摩尔质量为88 g?mol-1)
③讨论:用标准KMnO4溶液直接滴定菠菜研磨、浸泡、过滤得到的溶液结果可能偏高,原因是 。
小组成员在做草酸溶液与酸性高锰酸钾溶液反应实验时发现,溶液褪色先慢后快。
(1)上述H2C2O4溶液与酸性KMnO4溶液反应的离子方程为 。
(2)为了探究此反应速率由小变大的原因,甲同学做了如下实验(表中“一”表示未加入该试剂)。
| 实验 编号 | 反应温度 (利用水浴加热) | 稀硫酸 溶液 | MnSO4固体 | 0.10 mol/L KMnO4溶液 | 褪色 时间 |
| 1 | 750C | 一 | 一 | 1mL | 100s |
| 2 | 750C | 10滴 | 一 | 1mL | 40s |
| 3 | 750C | 10滴 | 加入少许 | 1mL | 3s |
II.乙同学查资料得知“菠菜中富含可溶性草酸盐和碳酸盐”, 决定用实验验证这一事实并检测草酸盐含量。进一步查阅资料得知,草酸(H2C2O4)是酸性强于醋酸的二元弱酸,对应的钙盐(CaC2O4)不溶于醋酸,能溶于强酸。
(1) 欲准确测定菠菜中草酸盐含量,回答有关问题:
①操作:取m g菠菜样品,将其中草酸盐转化为 CaC2O4 沉淀分离出来,用盐酸溶解后,溶液转入100mL容量瓶中加水配制成100mL溶液。每次移取25.00mL该溶液,用0.0100mol·L-1 KMnO4标准溶液滴定,滴定实验重复操作2 —3次。平均消耗标准溶液V mL。
②计算:菠菜中草酸盐(以C2O42-计)的质量分数为 。(只列式不计算,已知:C2O42-的的摩尔质量为88 g?mol-1)
③讨论:用标准KMnO4溶液直接滴定菠菜研磨、浸泡、过滤得到的溶液结果可能偏高,原因是 。
 已知电石中含有的杂质与水反应会生成H2S和PH3气体,某校研究性学习小组设计实验测定电石样品的纯度.经查阅有关资料得知:H2S、PH3与硫酸铜溶液反应的化学方程式分别是:
已知电石中含有的杂质与水反应会生成H2S和PH3气体,某校研究性学习小组设计实验测定电石样品的纯度.经查阅有关资料得知:H2S、PH3与硫酸铜溶液反应的化学方程式分别是:H2S+CuSO4═CuS↓+H2SO4
19PH3+56CuSO4+44H2O═11H3PO4+56H2SO4+32Cu↓+8Cu3P↓
(1)甲组同学设计如图装置测定电石样品的纯度.试填空:
①写出实验中生成乙炔的化学反应方程式:
CaC2+2H2O→Ca(OH)2+C2H2↑
CaC2+2H2O→Ca(OH)2+C2H2↑
.②电石充分反应后,在读数之前应
b c
b c
(填序号).a.立即读数;b.调节量筒与广口瓶中液面相平;c.待气体充分冷却到室温.
(2)乙组同学认为甲组同学设计的实验测定结果精确度不高,建议使用如图装置进行实验:

试回答下列问题:
①E中发生反应的化学方程式为
CH≡CH+2Br2→CHBr2CHBr2
CH≡CH+2Br2→CHBr2CHBr2
.②实验中需直接测定的数据有
a c
a c
.a.电石样品的质量 b.装置C的增重 c.装置E的增重 d.实验时的室温和压强
③实验时,待B中充分反应后,应打开活塞使A中贮存的空气缓缓进入B中,其目的是
使装置中生成的乙炔被E中溴的四氯化碳溶液充分吸收
使装置中生成的乙炔被E中溴的四氯化碳溶液充分吸收
.已知乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华.某校研究性学习小组为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生.该反应的离子方程式为
(2)向盛有少量乙二酸饱和溶液的试管中滴入用硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去,说明乙二酸具有
(3)将一定量的乙二酸放于试管中,按如图所示装置进行实验(夹持装置未标出):
实验发现,装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红,

据此,乙二酸分解的产物为
(4)该小组同学将2.52g草酸晶体(H2C2O4?2H2O)加入到100mL 0.2mol/L的NaOH溶液中充分反应,测得反应后溶液呈酸性,其原因是
查看习题详情和答案>>
(1)向盛有1mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生.该反应的离子方程式为
HCO3-+H2C2O4=HC2O4-+CO2↑+H2O
HCO3-+H2C2O4=HC2O4-+CO2↑+H2O
.(2)向盛有少量乙二酸饱和溶液的试管中滴入用硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去,说明乙二酸具有
还原性
还原性
(填“氧化性”、“还原性”或“酸性”),请配平该反应的离子方程式:2
2
MnO4-+5
5
H2C2O4+6
6
H+=2
2
Mn2++10
10
CO2↑+8
8
H2O(3)将一定量的乙二酸放于试管中,按如图所示装置进行实验(夹持装置未标出):
实验发现,装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红,

据此,乙二酸分解的产物为
CO、CO2、H2O
CO、CO2、H2O
.上述装置中,D的作用是除去混合气体中的CO2
除去混合气体中的CO2
. 装置F中发生反应的化学方程式为:CuO+CO
Cu+CO2
| ||
CuO+CO
Cu+CO2
.
| ||
(4)该小组同学将2.52g草酸晶体(H2C2O4?2H2O)加入到100mL 0.2mol/L的NaOH溶液中充分反应,测得反应后溶液呈酸性,其原因是
反应所得溶液为NaHC2O4溶液,由于HC2O4-的电离程度比水解程度大,导致溶液中c(H+)>c(OH-),所以溶液呈酸性
反应所得溶液为NaHC2O4溶液,由于HC2O4-的电离程度比水解程度大,导致溶液中c(H+)>c(OH-),所以溶液呈酸性
.