23(8分)现有分子式均为C3H6O2的四种有机物A、B、C、D,且分子中均含甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
|
|
NaOH溶液 |
银氨溶液 |
新Cu(OH)2 |
金属钠 |
|
A |
中和反应 |
-- |
溶解 |
产生氢气 |
|
B |
-- |
有银镜 |
加热后有红色沉淀 |
产生氢气 |
|
C |
水解反应 |
有银镜 |
加热后有红色沉淀 |
-- |
|
D |
水解反应 |
-- |
-- |
-- |
则A、B、C、D的结构简式分别为:
A__________,B_________,C__________,D__________。
24(10分)某厂以甘蔗为原料制糖,对产生的大量甘蔗渣按下图所示转化进行综合利用。其中B是A水解的最终产物;C的化学式为C3H6O3,一定条件下2个C分子间脱去2个水分子可生成一种六元环状化合物;D可使溴水褪色;H的三聚合物I也是一种六元环状化合物。(图中部分反应条件及产物没有列出)
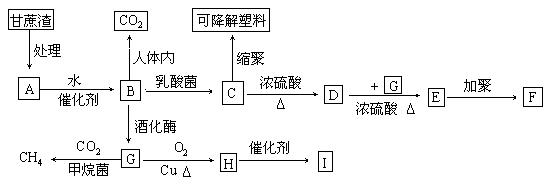 (1)写出下列物质的结构简式:
(1)写出下列物质的结构简式:
高分子化合物F_____________;六元环状化合物I_____________。
(2)C → D的反应类型为____________。D → E的反应类型为_____________。
(3)写出下列反应的化学方程式:A → B____________________________,
C →可降解塑料_____________________。
(4)H分子所含官能团的名称是__________,实验室中常用于检验该官能团的试剂的名称是(只写一种)__________________________。
(5)G转变成CH4的反应曾做过如下的同位素示踪实验(D、T为H的同位素):
 六、(本题包括2小题,共20分)
六、(本题包括2小题,共20分)
25(8分)已知pH = 2的高碘酸(H5IO6)溶液与pH = 12的NaOH溶液等体积混合,所得混合液显酸性;0.01 mol·L-1的碘酸(HIO3)或高锰酸(HMnO4)溶液与pH = 12的NaOH溶液等体积混合,所得混合液显中性。
请回答下列问题:
(1)高碘酸是_______(填写“强酸”或“弱酸”),理由是_____________________。
(2)已知高碘酸和硫酸锰(MnSO4)在溶液中反应生成高锰酸,碘酸和硫酸,此反应的氧化剂是_________,反应的离子方程式可表示为________________________________。
26(12分)在定量分析化学反应中各物质的计量关系时,往往可利用质量守恒、离子电荷守恒和得失电子守恒等规律将问题简单化。
现有单质铁溶于稀硝酸反应的化学方程式可表示为:
aFe + bNO3- + cH+ = d Fe2+ + fFe3+ + gNO↑+ hN2O↑+ kH2O
试回答下列问题:
(1)下列各种情况下的数学等量关系式为:
①b、c、d、f的数学关系式为_____________。
②d、f、g、h的数学关系式为_____________。
③c、g、h的数学关系式为_______________。
(2)若a =16时,Fe和稀硝酸全部反应,则b的取值范围是_____________,C的取值范围是________________。
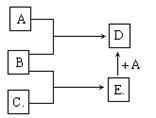
 2CuO、CuO +H2SO4 = CuSO4 + H2O。
2CuO、CuO +H2SO4 = CuSO4 + H2O。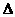 H1 =
-483.6 kJ·mol-1,则对于热化学方程式:2H2O(l)= 2H2(g)+ O2(g);
H1 =
-483.6 kJ·mol-1,则对于热化学方程式:2H2O(l)= 2H2(g)+ O2(g); D、
D、