24、(10分)合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响。合成氨反应的化学方程式为:N2(g)+3H2(g) 3NH3(g) △H=-92.2kJ/mol。合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。我国合成氨工业目前的生产条件为:催化剂-铁触媒,温度-400-500℃,压强-30-50MPa。
3NH3(g) △H=-92.2kJ/mol。合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。我国合成氨工业目前的生产条件为:催化剂-铁触媒,温度-400-500℃,压强-30-50MPa。
回答下列问题:
⑴ 合成氨工业中原料气压缩到30-50MPa的原因是 。从平衡移动原理分析,低温有利于原料气的转化,实际生产中采用400-500℃的高温,原因之一是考虑到催化剂的催化活性,原因之二是 。
⑵ 500℃、50MPa时,在容积为VL的容器中加入n mol N2、3n mol H2,反应达平衡后测得平衡常数为K,此时N2的转化率为x。则K和x的关系满足K= 。
⑶ 甲烷在高温下与水蒸气反应反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g)。部分物质的燃烧热数据如下表:
|
物 质 |
燃烧热(kJ·mol-1) |
|
H2(g) |
-285.8 |
|
CO(g) |
-283.0 |
|
CH4(g) |
-890.3 |
已知1mol H2O(g)转变为1mol H2O(l)时放出44.0 kJ热量。写出CH4和H2O在高温下反应的热化学方程式 。
⑷ 有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池。请写出该电池的正极反应式 。
22、(10分)2007年3月,温家宝总理在十届人大五次会议上指出要大力抓好节能降耗、保护环境。请你分析并回答下列问题:
(1)“绿色化学”的最大特点在于它是在始端就采用预防实际污染的科学手段,因而过程和终端均为零排放和零污染,具有“原子经济性”。下列化学反应不符合“绿色化学”思想的是 。
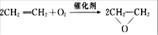 A.制备环氧乙烷:
A.制备环氧乙烷:

B.制备硫酸铜:Cu+2H2SO4 CuSO4+SO2↑+2H2O

C.制备甲醇: 2CH4+O2 2CH3OH
D.制备硝酸铜:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(2)冶金废水中含有[Au(CN)2]-,其电离出的CN-有毒,当与H+结合生成HCN时,其毒性更强。工业上处理这种废水是在碱性条件下,用NaClO将CN-氧化为CO32-和一种无毒气体,该反应的方程式为 ,在酸性条件下,ClO-也能将CN-氧化,但实际处理时却不在酸性条件下进行的主要原因是 。
(3)工业上目前使用两种方法制取乙醛--“乙炔水化法”和“乙烯氧化法”。下面两表提供生产过程中原料、反应条件、原料平衡转化率和产量等的有关信息:
|
|
乙炔水化法 |
乙烯氧化法 |
|
原料 |
乙炔、水 |
乙烯、空气 |
|
反应条件 |
HgSO4、100~125℃ |
PdCl2-CuCl2、100~125℃ |
|
平衡转化率 |
乙炔平衡转化率90%左右 |
乙烯平衡转化率80%左右 |
|
日产量 |
2.5吨(某设备条件下) |
3.6吨(相同设备条件下) |
表一:原料、反应条件、平衡转化率、日产量
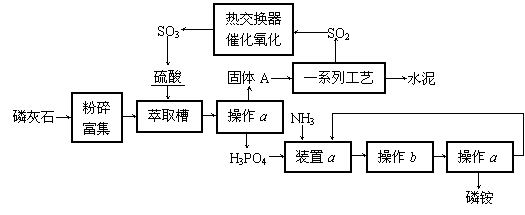
表二:原料来源生产工艺
|
|
原料生产工艺过程 |
|
乙炔 |
错误!嵌入对象无效。错误!嵌入对象无效。 |
|
乙烯 |
来源于石油裂解气 |
从两表中分析,现代工业上“乙烯氧化法”将逐步取代“乙炔水化法”的可能原因。
错误!未找到引用源。从产率和产量角度分析 。
错误!未找到引用源。从环境保护和能耗角度分析 。
18.通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实解释正确的是
|
|
现象 |
解释 |
|
A |
KI淀粉溶液中通入Cl2,溶液变蓝 |
Cl2能与淀粉发生显色反应 |
|
B |
浓HNO3在光照条件下变黄 |
浓HNO3不稳定,生成有色产物能溶于浓硝酸 |
|
C |
某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 |
说明该溶液中含有SO42- |
|
D |
向盐酸中加入浓硫酸时产生白雾 |
说明浓硫酸具有脱水性 |
 H++B(OH)4-,该反应中的碱是
(填H3BO3或H2O);
H++B(OH)4-,该反应中的碱是
(填H3BO3或H2O); R-X + Mg RMgX(格氏试剂)错误!未找到引用源。格氏试剂广泛用于有机合成,如在一定条件
R-X + Mg RMgX(格氏试剂)错误!未找到引用源。格氏试剂广泛用于有机合成,如在一定条件
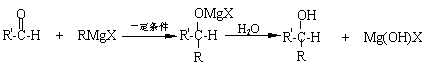 下能与醛中的羰基发生加成,生成物又可以发生水解生成醇:
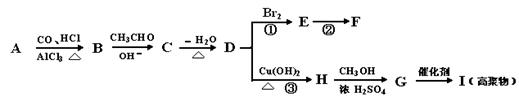
下能与醛中的羰基发生加成,生成物又可以发生水解生成醇: 因此上述反应常用于醛合成醇。现要合成
,请回答:
因此上述反应常用于醛合成醇。现要合成
,请回答:

 实验中每次对固体称量时须在冷却后
实验中每次对固体称量时须在冷却后 (3)众所周知,氢气燃烧生成水。然而,资料表明,
(3)众所周知,氢气燃烧生成水。然而,资料表明, 在一定条件下,可逆反应:N2+3H2 2NH3,DH<0,达到平衡时,当单独改变下列条件后,有关叙述错误的是
在一定条件下,可逆反应:N2+3H2 2NH3,DH<0,达到平衡时,当单独改变下列条件后,有关叙述错误的是