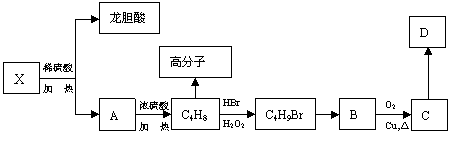
30.[化学-物质结构与性质] (13分)
|
 X、Y、Z三种元素,原子序数依次减小。X是第四周期主族元素,其部分电离能如图17所示;X、Y元素具有相同的最高正化合价;Z原子价电子排布式nsnnpn。回答下列问题:
X、Y、Z三种元素,原子序数依次减小。X是第四周期主族元素,其部分电离能如图17所示;X、Y元素具有相同的最高正化合价;Z原子价电子排布式nsnnpn。回答下列问题:
|
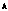
 (1)X原子的电子排布式为_______
____。
(1)X原子的电子排布式为_______
____。





















|
|
























 (2)电负性:X ______Y(填“>”、“=”或“<”)。
(2)电负性:X ______Y(填“>”、“=”或“<”)。





|



















 (3)元素Z的一种氢化物(化学式为Z2H4)是重要的
(3)元素Z的一种氢化物(化学式为Z2H4)是重要的













 化工原料。有关Z2H4分子的说法正确的是______(填字母)。
化工原料。有关Z2H4分子的说法正确的是______(填字母)。






|
















 A.分子中含有氢键
A.分子中含有氢键







|


















 B.和O2分子具有相同的电子数
B.和O2分子具有相同的电子数
|
|
|
|
|
|
|
|
|
|
 C.含有4个σ键和1个π键
C.含有4个σ键和1个π键
 D.Z的原子与氢原子形成的化学键可以旋转
D.Z的原子与氢原子形成的化学键可以旋转
(4)X的氧化物与钛(Ti)的氧化物相互作用,能形成钛酸盐,
其晶体结构示意图如图18所示(X、Ti和O三种元素对应的离子
分别位于立方体的体心、顶点和面心)。该晶体中,钛离子和周围
_________(填数字)个氧离子相紧邻。
(5)NH4Cl晶体中含有多种化学键,其中一定不含有的化学键是_____(填字母)。
A.离子键 B.非极性键 C.配位键 D.金属键
25.(15分)粗盐提纯的研究。
[有关资料]
|
化学式 |
CaCO3 |
CaSO4 |
Ca(OH)2 |
MgCO3 |
Mg(OH)2 |
|
Ksp |
2.8×10一9 |
9.1×10一6 |
1.0×10一4 |
3.5×10一5 |
1.6×10一11 |
某研究性学习小组对粗盐的提纯和检验进行研究,并提出一些新的方案。已知该粗盐样品中主要含有不溶性杂质、Mg2+、Ca2+等(忽略SO42-的存在),该小组设计流程如下:
[设计除杂过程]

(1)操作①中需要使用的玻璃仪器有(i) 、(ii) 。操作②的名称为(iii) ,若在操作②结束后发现溶液B略有浑浊,应采取的措施是(iv) ;
(2)混合液A的主要成分是 。(填化学式)
[检验除杂效果]
(3)为检验溶液B中Mg2+、Ca2+是否除尽,通常分别取少量溶液B于两支试管中。进行如下实验:
步骤一:检验Mg2+是否除尽。向其中一支试管中加入 溶液(填化学式),如果没有沉淀生成,则Mg2+已除尽。
步骤二:检验Ca2+是否除尽。向另一支试管中加入某溶液,如果没有沉淀生成,则Ca2+已除尽,效果最好的是 (填字母)。
A.Na2CO3 B.Na2SO4 C.NaOH
[获取纯净食盐]
(4)对溶液B加热并不断滴加l mol·L-1的盐酸溶液,同时用pH试纸检测溶液,直至pH=5时停止加盐酸,得到溶液C。该操作的目的是 ;用试纸测pH值的实验操作为 。
(5)将溶液C倒入 (填仪器名称)中,加热蒸发并用玻璃棒不断搅拌,直到 时(填现象),停止加热。
[问题讨论]
(6)进行操作②前,需先加热,其目的是
,该操作中控制溶液pH=12可确保Mg2+除尽,根据提供的数据计算,此时溶解B中Mg2+物质的量浓度为 。
24.(15分)氢氧化镁用于制药工业,还是重要的绿色阻燃剂。
I、治疗胃酸过多药物Stmoache的有效成分为Mg(OH)2。
(1)该药物治疗胃酸(主要成分为盐酸)过多症时反应的离子方程式:
________ _____。
Ⅱ、已知:Mg (s)+2H2O(g)=Mg(OH)2(s)+H2(g) △H1=-441kJ·mol-1
H2O(g)=H2(g)+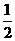 O2(g) △H2=+242kJ·mol-1
O2(g) △H2=+242kJ·mol-1
Mg(s)+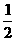 O2(g)=MgO(s) △H3=-602kJ·mol-1
O2(g)=MgO(s) △H3=-602kJ·mol-1
(2)氢氧化镁分解的热化学方程式是_______________________________________。
(3)氢氧化镁可以作为阻燃剂的原因____________________。(写一条即可)
Ⅲ、某工厂用六水合氯化镁和粗石灰制取的氢氧化镁含有少量氢氧化铁杂质,通过如下流程进行提纯精制,获得阻燃剂氢氧化镁。

(4)步骤②中分离操作的名称是______ _______。
(5)步骤①中的反应如下:6Fe(OH)3 +S2O42-+2OH- =6Fe(OH)2 +2SO42-+4H2O。
每消耗0.1mol保险粉(Na2S2O4)时,转移电子的数目是 NA。
(6)已知EDTA只能与溶液中的Fe2+反应生成易溶于水的物质,不与Mg(0H)2反应。虽然Fe(OH)2难溶于水,但步骤②中随着EDTA的加入,最终能够将Fe(OH)2除去并获得纯度高的Mg(OH)2。请从沉淀溶解平衡的角度加以解释。
答:_____________________________________________________________________。
Ⅳ、为研究不同分离提纯条件下所制得阻燃剂的纯度从而确定最佳提纯条件,某研究小组各取等质量的下列4组条件下制得的阻燃剂进行含铁量的测定,结果如下:
|
精制阻燃剂的条件 |
阻燃剂铁含量 |
|||
|
序号 |
提纯体系温度T/℃ |
加入EDTA质量(g) |
加入保险粉质量(g) |
W(Fe)/(10-4g) |
|
1 |
40 |
0.05 |
0.05 |
7.63 |
|
2 |
40 |
0.05 |
0.10 |
6.83 |
|
3 |
60 |
0.05 |
0.10 |
6.83 |
|
4 |
60 |
0.10 |
0.10 |
6.51 |
(7)若不考虑其它条件,根据上表数据,制取高纯度阻燃剂最佳条件是______(填字母)
①40℃ ②60℃ ③EDTA质量为0.05g ④EDTA质量为0.10g
⑤保险粉质量为0.05g ⑥保险粉质量为0.10g
A.①③⑤ B.②④⑥ C.①④⑥ D.②③⑤
12.某无色溶液含有①Na+ 、②Ba2 +、 ③Cl一、 ④Br一、⑤SO32一、⑥SO42一 离子中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
|
步骤 |
操作 |
现象 |
|
(1) |
用pH试纸检验 |
溶液的pH大于7 |
|
(2) |
向溶液中滴加氯水,再加入CCl4振荡,静置 |
CCl4层呈橙色 |
|
(3) |
向所得水溶液中加入Ba(NO3)2溶液和稀HNO3 |
有白色沉淀产生 |
|
(4) |
过滤,向滤液中加入AgNO3溶液和稀HNO3 |
有白色沉淀产生 |
下列结论正确的是
A.肯定含有的离子是①④⑤ B.肯定没有的离子是②⑥
C.不能确定的离子是① D.不能确定的离子是③⑤
 A.用电解法精炼精铜时,粗铜作阳极,纯铜作阴极
A.用电解法精炼精铜时,粗铜作阳极,纯铜作阴极 [化学--有机化学基础](13分)
[化学--有机化学基础](13分)