28.(14分)随着能源问题的进一步突出,利用热化学循环制氢的研究受到许多发达国家的青睐。最近的研究发现,复合氧化物铁酸锰(MnFe2O4)也可以用于热化学循环分解水制氢,MnFe2O4的制备流程如下:

⑴已知滤液中不含Fe和Mn两种元素,则投入原料Fe(NO3)n和Mn(NO3)2的物质的量之比应为__________。
⑵B操作中“连续搅拌”的目的是___________ _______________ ;C操作中检验沉淀是否洗涤干净的方法是_____________________________________。
⑶利用MnFe2O4热化学循环制氢的反应可表示为(以下反应过程中Mn的化合价不变):
MnFe2O4 MnFe2O4-x+
MnFe2O4-x+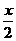 O2↑ MnFe2O4-x+xH2O→MnFe2O4+xH2↑
O2↑ MnFe2O4-x+xH2O→MnFe2O4+xH2↑
|
①若MnFe2O4-x中X=0.8,则MnFe2O4-x中Fe占全部铁元素的百分率为________。
②该热化学循环制氢的优点有(答两点即可)_________________________________________
__________________________________。
③该热化学循环法制氢尚有不足之处,进一步改进的研究方向是_________________。

 ①将0.1 mol/L的NaOH溶液与0.5 mol/L的CuSO4溶液等体积混合制得氢氧化铜浊液,用于检验醛基 ②实验室制硝基苯要在水浴的热水中插入温度计 ③实验室制乙烯时温度计水银球要插入反应液中并缓慢升高温度到170℃ ④冷凝管在使用时,为了确保冷凝效果必须采取逆流的方式 ⑤分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 ⑥蔗糖水解实验完成后再加入新配制的银氨溶液即可检验生成的醛基
①将0.1 mol/L的NaOH溶液与0.5 mol/L的CuSO4溶液等体积混合制得氢氧化铜浊液,用于检验醛基 ②实验室制硝基苯要在水浴的热水中插入温度计 ③实验室制乙烯时温度计水银球要插入反应液中并缓慢升高温度到170℃ ④冷凝管在使用时,为了确保冷凝效果必须采取逆流的方式 ⑤分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 ⑥蔗糖水解实验完成后再加入新配制的银氨溶液即可检验生成的醛基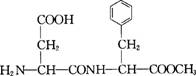
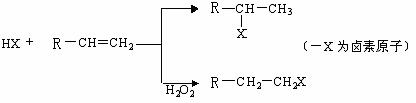
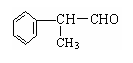
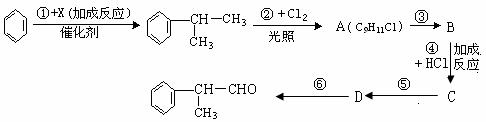
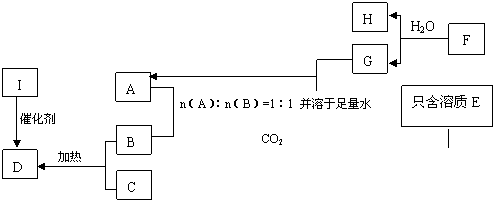 (15分)常温下,A、B、C是三种常见的固体化合物;C、I、H均为常见的X2Y2型化合物,并且I为液体,H为气体;构成A和F的阳离子的质子数之和为31,G为微溶物。其中A与C按任意比例混合,溶于足量的水中,得到的溶质也只含有一种,并有无色、无味的气体D放出。它们之间有如下的转化关系:(部分物质未写出)
(15分)常温下,A、B、C是三种常见的固体化合物;C、I、H均为常见的X2Y2型化合物,并且I为液体,H为气体;构成A和F的阳离子的质子数之和为31,G为微溶物。其中A与C按任意比例混合,溶于足量的水中,得到的溶质也只含有一种,并有无色、无味的气体D放出。它们之间有如下的转化关系:(部分物质未写出)


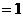 的H
的H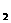 SO
SO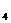 ,则所得溶液中各离子浓度由大到小的排列顺序为
_______
。
,则所得溶液中各离子浓度由大到小的排列顺序为
_______
。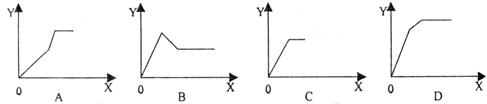
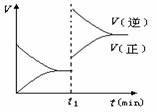 12.下图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或者增大压强.速率的变化都符合的示意图的反应是
12.下图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或者增大压强.速率的变化都符合的示意图的反应是 2SO3(g);△H<0
2SO3(g);△H<0