15.(8分) 在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
|
时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
|
n(NO)(mol) |
0.020 |
0.01. |
0.008 |
0.007 |
0.007 |
0.007 |
⑴写出该反应的平衡常数表达式:K= 。
 已知:
已知: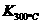 >
> ,则正反应是 热反应。
,则正反应是 热反应。
⑵右图中表示NO2的变化的曲线是 。
用O2表示从0-2s内该反应的平均速率v= 。
⑶能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆 (NO)=2v正 (O2) d.容器内密度保持不变
⑷为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
9.某些化学键键能数据如下:
|
化学键 |
H-H |
C1-Cl |
H-Cl |
键能 |
436 |
243 |
431 |
则下列热化学方程式不正确
A. H2(g)+
H2(g)+  Cl2(g)
Cl2(g) HCl(g);
HCl(g); = -91.5
= -91.5
B. H2(g)+ Cl2(g) 2HCl(g);
2HCl(g); = -183
= -183
C. H2(g)+
H2(g)+  Cl2(g)
Cl2(g) HCl(g);
HCl(g); = +91.5
= +91.5
D.2HCl(g) H2(g)+ Cl2(g);
H2(g)+ Cl2(g); = +183
= +183
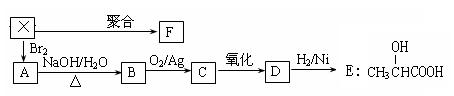


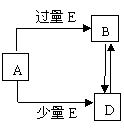 (8分)已知A、B、D、E均为中学化学常见单质或化合物,它
(8分)已知A、B、D、E均为中学化学常见单质或化合物,它 用铅蓄电池电解苦卤水 (含C1-、Br-、Na+、Mg2+)的装置如图所示 (a、b为石墨电极)。下列说法中正确的是
用铅蓄电池电解苦卤水 (含C1-、Br-、Na+、Mg2+)的装置如图所示 (a、b为石墨电极)。下列说法中正确的是