⑶ P(s) + 3/4O2(g) == 1/2 P2O3(s);△H = -(20X-Y) KJ/mol
15.(05江苏.21)通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
|
化学键 |
Si-O |
Si-Cl |
H-H |
H-Cl |
Si-Si |
Si-C |
|
键能/kJ·mol-1 |
460 |
360 |
436 |
431 |
176 |
347 |
请回答下列问题:
(1)比较下列两组物质的熔点高低(填“>”或“<”
SiC Si; SiCl4 SiO2
 (2)右图立方体中心的“●”表示硅晶体中的一个原子,
(2)右图立方体中心的“●”表示硅晶体中的一个原子,
请在立方体的顶点用“●”表示出与之紧邻的硅原子。
(3)工业上高纯硅可通过下列反应制取:
SiCl4(g) + 2H2(g) 高温 Si(s) + 4 HCl(g)
该反应的反应热△H = kJ/mol.
[解析]:(1)原子晶体键能越高,则物质的熔点越高;原子晶体熔点大于分子晶体,则答案可知。(2)略
(3)根据化学反应的本质反应物的总键能减去生成物总键能就等于反应热,
SiCl4(g) + 2H2(g) 高温 Si(s) + 4 HCl(g)
△H =4×347KJ/mol+2×436 KJ/mol-2×176 KJ/mol-4×431 KJ/mol=+236 KJ/mol
[答案]:
 (1)> < (2)如图
(1)> < (2)如图
(3)+236

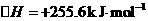
 O2(g)→3H2(g)+2CO(g)
O2(g)→3H2(g)+2CO(g)
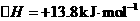

 O2(g)=H2O(l) ΔH 3=-285.8kJ/mol
O2(g)=H2O(l) ΔH 3=-285.8kJ/mol 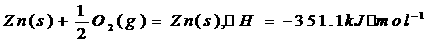



 N2(g)+
N2(g)+ H2(g)=NH3(1); △H=(h+c-a) kJ·mol-1
H2(g)=NH3(1); △H=(h+c-a) kJ·mol-1