网址:http://m.1010jiajiao.com/timu3_id_54218[举报]
(常州市第二中学09高三化学期中质量检测试卷)膳食纤维具有突出的保健功能,人体的“第七营养素”木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如右图所示.下列有关芥子醇的说法正确的是
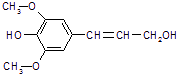 A.芥子醇的分子式是C11H14O4,属于芳香烃
A.芥子醇的分子式是C11H14O4,属于芳香烃
B.芥子醇分子中所有碳原子不可能在同一平面
C.芥子醇不能与FeCl3溶液发生显色反应
D.芥子醇能发生的反应类型有氧化、取代、加成
查看习题详情和答案>>某中学化学探究小组通过查阅相关资料,对蛭石的组成进行了实验探究.
I、相关资料:①蛭石的成分可看成是由MgO、Fe2O3、Al2O3、SiO2组成
②氢氧化物开始沉淀及沉淀完全时的pH
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 | Al(OH)3 |
| 沉淀的pH范围 | 1.5-4.1 | 9.4-12.4 | 3.3-5.2 |

Ⅲ、实验数据:
①矿石样品质量为:8.22g ②每次转化所得固体成分只有一种
请你根据以上内容和中学化学知识回答以下问题
(1)写出由D制一种红色颜料的化学方程式:
| ||
| ||
(2)工业上的耐火材料通常由F及滤液E进一步转化而成,请你分析滤液E中可能含有成分,设计一个从滤液E制取耐火材料的实验方法:
(3)滤液B和NaOH溶液反应时,应控制溶液的pH在7-8之间,这是因为:
(4)通过计算,写出用氧化物的形式表示蛭石组成的化学式
[江苏省南通中学2008学年度第一学期期末复习高三化学 ].某化学课外活动小组研究乙醇氧化的实验并验证其产物,设计了甲、乙、丙三套装置(图中的夹持仪器均未画出,“△”表示酒精灯热源),每套装置又可划分为①、②、③三部分。仪器中盛放的试剂为:a-无水乙醇(沸点:78 ℃);b-铜丝;c-无水硫酸铜;d-新制氢氧化铜悬浊液。
(1)简述两套方案各自的优点:甲:_________________、_________________________,
乙:___________________
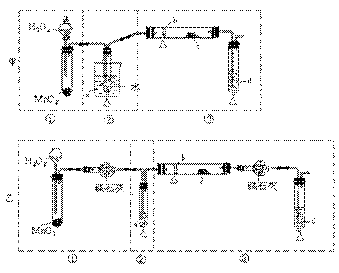 (2)集中两套方案的优点,组成一套比较合理完善的实验装置,可按气流由左至右的顺序表示为________________(例如甲①,乙②)
(2)集中两套方案的优点,组成一套比较合理完善的实验装置,可按气流由左至右的顺序表示为________________(例如甲①,乙②)
(3)若要保证此实验有较高的效率,还需补充的仪器有__________。理由______。
(4)实验中能验证乙醇氧化产物的实验现象是_______________。
(5)装置中,若撤去第①部分,其它操作不变,则无水硫酸铜无明显变化,其余现象与(4)相同,推断燃烧管中主要反应的化学方程式____________。
查看习题详情和答案>>(08黄桥中学模拟) 石油化工是江苏省的支柱产业之一。聚氯乙烯是用途十分广泛的石油化工产品,某化工厂曾利用下列工艺生产聚氯乙烯的单体氯乙烯:
CH2=CH2+Cl2→CH2CI―CH2C1…………………①
CH2Cl―CH2C1→CH2=CHCl+HCl………………②
请回答以下问题:
(1)已知反应①中二氯乙烷的产率)产率=![]() ×100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8t乙烯可制得氯乙烯 t,同时得到副产物氯化氢 t。(计算结果保留1位小数)
×100%)为98%,反应②中氯乙烯和氯化氢的产率均为95%,则2.8t乙烯可制得氯乙烯 t,同时得到副产物氯化氢 t。(计算结果保留1位小数)
(2)为充分利用副产物氯化氢,该工厂后来将下列反应运用于生产:
2CH2=CH2+4HCl+O2→2CH2Cl-CH2Cl+2H2O…………③
由反应①、③获得二氯乙烷,再将二氯乙烷通过反应②得到氯乙烯和副产物氯化氢,副产物氯化氢供反应③使用,形成了新的工艺。
由于副反应的存在,生产中投入的乙烯全部被消耗时,反应①、③中二氯乙烷的产率依次为a%、c%;二氯乙烷全部被消耗时,反应②中氯化氢的产率为b%。试计算:反应①、③中乙烯的投料比为多少时,新工艺既不需要购进氯化氢为原料,又没有副产物氯化氢剩余(假设在发生的副反应中既不生成氯化氢,也不消耗氯化氢)。
查看习题详情和答案>>某中学化学探究小组通过查阅相关资料,对蛭石的组成进行了实验探究.
I、相关资料:①蛭石的成分可看成是由MgO、Fe2O3、Al2O3、SiO2组成
②氢氧化物开始沉淀及沉淀完全时的pH
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 | Al(OH)3 |
| 沉淀的pH范围 | 1.5-4.1 | 9.4-12.4 | 3.3-5.2 |
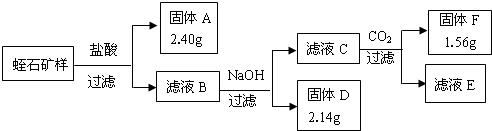
Ⅲ、实验数据:
①矿石样品质量为:8.22g ②每次转化所得固体成分只有一种
请你根据以上内容和中学化学知识回答以下问题
(1)写出由D制一种红色颜料的化学方程式:______
(2)工业上的耐火材料通常由F及滤液E进一步转化而成,请你分析滤液E中可能含有成分,设计一个从滤液E制取耐火材料的实验方法:______
(3)滤液B和NaOH溶液反应时,应控制溶液的pH在7-8之间,这是因为:______
(4)通过计算,写出用氧化物的形式表示蛭石组成的化学式______.