17.(10分)合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料。从天然气获得合成气过程中可能发生的反应有:
① CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+206.1 kJ/mol
CO(g)+3H2(g) ΔH1=+206.1 kJ/mol
② CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH2=+247.3 kJ/mol
2CO(g)+2H2(g) ΔH2=+247.3 kJ/mol
③ CO(g)+H2O(g) CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
请回答下列问题:
⑴ 在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示。反应进行的前5 min内,v(H2)= ▲ ;10 min时,改变的外界条件可能是 ▲ 。

⑵ 如图2所示,在甲、乙两容器中分别充入含等物质的量的CH4和CO2混合气体,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间变化的图像如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图像。

⑶ 反应③中ΔH3= ▲ 。800℃时,反应③的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
|
CO |
H2O |
CO2 |
H2 |
|
0.5 mol |
8.5 mol |
2.0 mol |
2.0 mol |
此时反应③中正、逆反应速率的关系式是 ▲ (填字母)。
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断
 。物质A在体内脱氢酶的作用下会氧化为有害物质GHB。下图是关于物质A的一种制备方法及由A引发的一系列化学反应。
。物质A在体内脱氢酶的作用下会氧化为有害物质GHB。下图是关于物质A的一种制备方法及由A引发的一系列化学反应。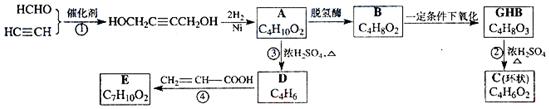
 请回答下列问题:
请回答下列问题: 结构),它的结构简式为__ ____▲ _________。
结构),它的结构简式为__ ____▲ _________。 d.减少资源消耗,增加资源的重复使用、资源的循环再生
d.减少资源消耗,增加资源的重复使用、资源的循环再生 2H2↑+O2↑
2H2↑+O2↑ 2H2↑+O2↑
2H2↑+O2↑ 2H2↑+O2↑
2H2↑+O2↑ CO+3H2
CO+3H2 MnFe2O4-X+ O2
MnFe2O4-X+ O2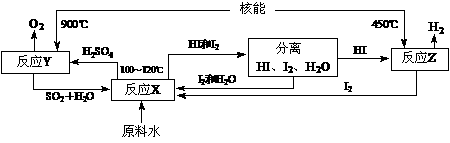
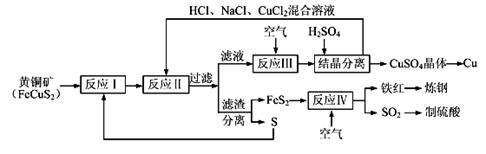
 8Cu+4FeO+2Fe2O3+16SO2,下列有关该反应的说法正确的是 ▲ (填字母)。
8Cu+4FeO+2Fe2O3+16SO2,下列有关该反应的说法正确的是 ▲ (填字母)。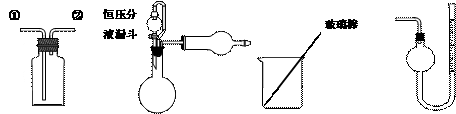
 方案甲:通过测量试样与碱反应生成的氢气体积来实现探究目标。
方案甲:通过测量试样与碱反应生成的氢气体积来实现探究目标。 Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0),某温度、压强下,将一定量的反应物通入密闭容器进行以上的反应,下列叙述正确的是
Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0),某温度、压强下,将一定量的反应物通入密闭容器进行以上的反应,下列叙述正确的是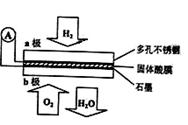 某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2=2H2O,下列有关说法正确的是
某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2=2H2O,下列有关说法正确的是