22.(11分)某探究小组同学用金属铝分别与稀盐酸或稀硫酸反应的方法研究金属与不同酸反应的差异及影响反应速率的因素。
实验药品:2. 0moL/L盐酸、4. 0mol/L盐酸、2 .0mol/L硫酸、4.0mol/L硫酸,质量相同的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50. 0mL,金属用量均为9. 0g。
(Ⅰ)甲同学用铝片分别和稀盐酸、稀硫酸反应,实验及其现象如下:
|
反应进程(分钟) |
1 |
2 |
5 |
15 |
20 |
|
4.0mol/L盐酸 |
少量气泡 |
较多气泡 |
大量气泡 |
反应剧烈 |
反应结束 |
|
2.0mol/L硫酸 |
无明显现象 |
极少量气泡 |
少量气泡 |
||
|
4.0mol/L硫酸 |
无明显现象 |
少量气泡 |
有比较连续的气泡 |
请回答:
(1)写出铝与盐酸反应的离子方程式 。
(2)反应1~15min内,铝与盐酸的反应速率逐渐加快,其原因是
。
(3)以上探究铝与稀盐酸、稀硫酸反应速率有差异,你认为其原因有哪些可能?请提出你的假设(说出2种可能): 。
(Ⅱ)(1)乙同学设计了如下影响反应速率因素的实验(温度控制为25℃和35℃)。请你根据实验目的帮助该同学完成以下实验设计表(用量:酸均为50. 0mL、铝为9. 0g过量):
|
实验目的 |
实验 编号 |
温度 |
金属铝 形态 |
盐酸浓度 /mol·L-1 |
|
1. 实验①和②探究盐酸浓度对该反应速率的影响; 2. 实验①和③探究温度对该反应速率的影响; 3. 实验①和④探究金属规格(铝片、铝粉)对该反应速率的影响。 |
① |
25˚C |
铝片 |
4. 0 |
|
② |
|
|
|
|
|
③ |
|
|
|
|
|
④ |
|
|
|
 (2)右图为实验①的“V(H2) -t”曲线图,若
(2)右图为实验①的“V(H2) -t”曲线图,若
上述反应浓度减少一倍,速率是原来的1/2;温
度每升高10 ℃,反速率是原来的2倍。请在
答题卡的座标中画出实验②和实验③的“V(H2) -t”
曲线图。
21.(12分)J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。
(1)M的离子结构示意图为_____;元素T在周期表中位于第_____族。
(2)J和氢组成的化合物分子有6个原子,其结构简式为______。
(3)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为_____。
(4)L的最简单气态氢化物甲的水溶液显碱性。
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2 的清除剂,所发生反应的产物不污染环境,其化学方程式为______。
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是_______(选填序号)。
|
选项 |
a |
b |
c |
d |
|
x |
温度 |
温度 |
加入H2的物质的量 |
加入甲的物质的量 |
|
y |
甲的物质的量 |
平衡常数K |
甲的转化率 |
生成物物质的量总和 |
(5)由J、R形成的液态化合物JR2 0.2mol在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ。 该反应的热化学方程式为________。
20、(10分)几种中学化学常见的单质及其化合物相互转化的关系图如下:
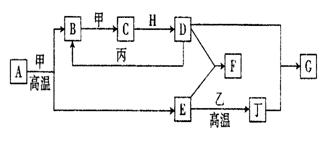
可供参考的信息有:
①甲、乙、丙、丁为单质,其余为化合物
② A由X和Y两种元素组成,其原子个数比为l︰2,元素质量之比为7︰8。
③ B气体是引起酸雨的主要物质,H常温下为无色无味的液体,E常用作红色油漆和涂料。
试根据上述信息回答下列问题:
(1)A的化学式为 ,每反应lmol的A转移的电子数为 mol;
(2)F与丁单质也可以化合生成G,试写出该反应的离子方程式: ;
(3)少量F的饱和溶液分别滴加到下列物质中,得到三种分散系①、②、③。
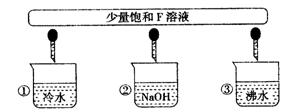
试将①、②、③填人下列方框中:
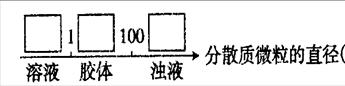
|
(4)化合物M与H组成元素相同,可以将G氧化为F,且不引进新的离子。试写出M在酸性环境下将G氧化为F的离子方程式:
19.(13分)某研究小组探究MgCl2和AlCl3溶液加入氢氧化钠溶液生成沉淀及沉淀溶解的情况,实验过程中可能用到的仪器与药品如下:
过滤装置,试管,烧杯,滴管,0.5mol/L MgCl2、AlCl3各100mL,酚酞溶液,石蕊溶液,0.1mol/L NaOH溶液,6mol/L NaOH溶液,0.1 mol/L盐酸
探究一:实验开始时产生沉淀的成份
[假设一]实验开始时产生的沉淀是Mg(OH)2
[假设二]
[假设三]实验开始时产生的沉淀是Al(OH)3和Mg(OH)2
基于假设二成立,请利用下表完成实验过程:
|
实验步骤 |
预期实验现象 |
预期实验结论 |
|
|
|
|
|
|
|
|
|
|
|
|
探究二:何时产生氢氧化镁沉淀
|
实验步骤 |
实验现象 |
实验结论 |
|
①另取0.5mol/L MgCl2、AlCl3溶液各30mL于不同烧杯中 |
|
|
|
②向0.5mol/L AlCl3溶液中逐滴加入NaOH溶液至刚好反应完全 |
产生沉淀,沉淀增多,沉淀溶解,沉淀消失 |
产生氢氧化铝沉淀,加过量的氢氧化钠溶液后氢氧化铝又溶解。 |
|
③将MgCl2溶液全部倒入到②反应后的溶液中。 |
产生大量白色沉淀 |
|
请用离子方程式表示上述实验步骤③的结论

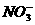
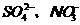
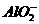 、Na+、
、Na+、 、
、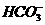
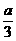 mol ④
mol ④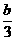 mol ⑤0 ⑥(4a- b)mol
mol ⑤0 ⑥(4a- b)mol