21、(10分)近年来北京市汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物。
(1)汽车内燃机工作时引起反应:N2(g)+O2(g)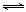 2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则T ℃时该反应的平衡常数K=
。(计算结果保留小数点后两位数字)
2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则T ℃时该反应的平衡常数K=
。(计算结果保留小数点后两位数字)
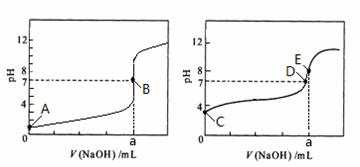
(2)一定量的NO发生分解的过程中,NO的转化率随时间变化的曲线如右图所示。
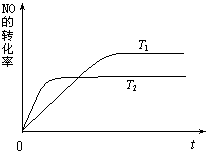
①反应 2NO(g) 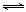 N2(g)+O2(g)为(填“吸热”或“放热”)
反应。
N2(g)+O2(g)为(填“吸热”或“放热”)
反应。
|
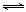 N2(g)+O2(g) 已达到平衡的是(填序号) 。
N2(g)+O2(g) 已达到平衡的是(填序号) 。
a.容器内的压强不发生变化 b.NO、N2、O2的浓度保持不变
c.NO分解的速率和NO生成的速率相等 d.单位时间内分解4 mol NO,同时生成2 mol N2
(3)①当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染。
已知:CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ·mol-1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H2
CH4(g)+2NO2(g) = N2(g)+CO2(g)+2H2O(g) △H3=-867 kJ·mol-1
△H2= 。
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NOx)转化为无毒气体,
该反应的化学方程式为 。
14、几种短周期元素部分性质的数据见下表:
|
元素性质 |
元素编号 |
|
① ② ③ ④ ⑤ ⑥ ⑦ |
|
|
原子半径 |
0.74 1.60 1.52 1.10 0.99 1.86 0.75 |
|
最高正化合价 |
无
+2 +1 +5 +7 +1 +5 |
|
最低负化合价 |
-2 无 无 -3 -1 无 -3 |
下列说法正确的是
A.③、⑥号元素都是金属元素
B.⑤的单质(M)与水反应的化学方程式为:2M + 2H2O= 2MOH + H2↑
C.⑥是该周期元素中原子半径最小的元素
D.①、⑥号元素只能形成一种白色化合物
13、下述实验能达到预期目的的是
|
编号 |
实验内容 |
实验目的 |
|
A |
将SO2通入酸性KMnO4溶液中 |
证明SO2具有氧化性 |
|
B |
将Cl2通入NaBr溶液中 |
比较氯与溴的氧化性强弱 |
|
C |
通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失 |
证明此溶液是Na2SiO3溶液 |
|
D |
分别向2支试管中加入相同体积但不同浓度的H2O2溶液,再向其中1支加入少量MnO2 |
研究催化剂对H2O2分解速率的影响 |
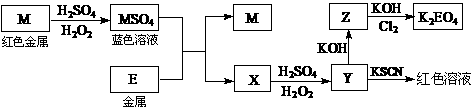
 ⑷由E制备的E(C2H5)2的结构如右图,其中氢原子的化学环境完全相同。但早期人们却错误地认为它的结构为:
⑷由E制备的E(C2H5)2的结构如右图,其中氢原子的化学环境完全相同。但早期人们却错误地认为它的结构为: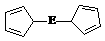 。核磁共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有 种峰,错误的结构有 种峰。
。核磁共振法能够区分这两种结构。在核磁共振氢谱中,正确的结构有 种峰,错误的结构有 种峰。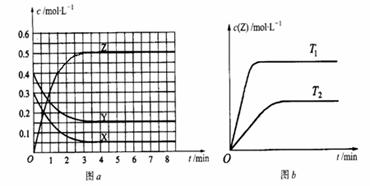 温度为T0时,在容积固定的容器中发生反应,各物质的浓度随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应,Z的浓度随时间变化的关系如图b所示。下列叙述正确的是
温度为T0时,在容积固定的容器中发生反应,各物质的浓度随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应,Z的浓度随时间变化的关系如图b所示。下列叙述正确的是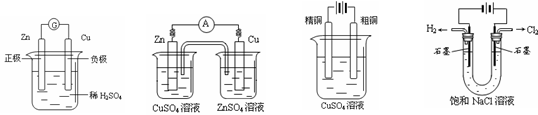 下图有关电化学的示意图正确的是
下图有关电化学的示意图正确的是