0 42802 42810 42816 42820 42826 42828 42832 42838 42840 42846 42852 42856 42858 42862 42868 42870 42876 42880 42882 42886 42888 42892 42894 42896 42897 42898 42900 42901 42902 42904 42906 42910 42912 42916 42918 42922 42928 42930 42936 42940 42942 42946 42952 42958 42960 42966 42970 42972 42978 42982 42988 42996 447348
 PCl5 ,各物质均为气态。达平衡后,PCl5为0.8mol。若此时再移走2molPCl3和1molCl2 ,相同温度下达到平衡,PCl5的物质的量为
PCl5 ,各物质均为气态。达平衡后,PCl5为0.8mol。若此时再移走2molPCl3和1molCl2 ,相同温度下达到平衡,PCl5的物质的量为  bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的55%,则
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的55%,则 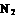 +3
+3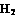
 2
2 ,则在电化学合成氨的过程中,阴极反应式为
;
,则在电化学合成氨的过程中,阴极反应式为
;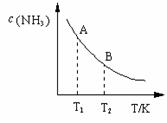 (3)在一定条件下,将l mol N2 与3 mol H2 混合于一个10 L密闭容器中,反应达到平衡时,A点混合气体中氨占25%,试回答:
(3)在一定条件下,将l mol N2 与3 mol H2 混合于一个10 L密闭容器中,反应达到平衡时,A点混合气体中氨占25%,试回答: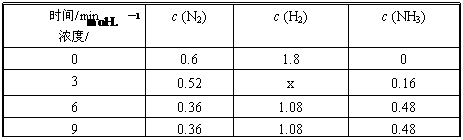

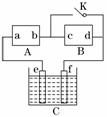 22、右图A为直流电源,B为渗透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B 上的 C
点显红色,请填空:
22、右图A为直流电源,B为渗透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B 上的 C
点显红色,请填空: H3O++OH- ΔH>0
H3O++OH- ΔH>0