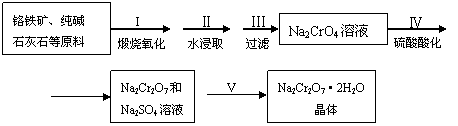
18.(12分)工业合成氨与制备硝酸一般可连续生产,流程如下:
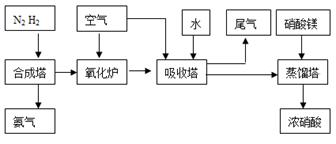
(1)某温度下体积为200L的氨合成塔中,测得如下数据:
 |
0 |
1 |
2 |
3 |
4 |
|
N2 |
1.500 |
1.400 |
1.200 |
C1 |
C1 |
|
H2 |
4.500 |
4.200 |
3.600 |
C2 |
C2 |
|
NH3 |
0 |
0.200 |
0.600 |
C3 |
C3 |
根据表中数据计算0-2小时内N2的平均反应速率 mol·L-1·h-1
若起始时与平衡时的压强之比为a,则N2的转化率为 (用含a的代数式表示)
(2)希腊阿里斯多德大学的 George Marnellos 和 Michael Stoukides,发明了一种合成氨的新方法(Science,2,Oct.1998, p98),在常压下,把氢气和用氦气稀释的氮气分别通入一个加热到570℃的电解池,利用能通过氢离子的多孔陶瓷固体作电解质,氢气和氮气在电极上合成了氨,转化率达到78%,试写出电解池阴极的电极反应式 。
(3)已知:N2(g)+O2(g) =2NO(g); △H=180.5kJ/mol
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ;△H=-905kJ/mol
2H2(g)+O2(g)=2H2O(g) ; △H=-483.6kJ/mol
则N2(g)+3H2(g) 2NH3(g) 的 △H=_________________。
2NH3(g) 的 △H=_________________。
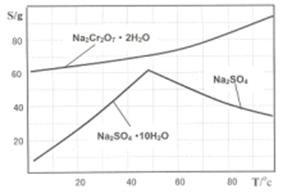
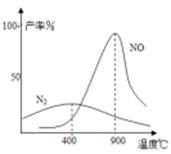 (4)氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图):
(4)氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图):
4NH3+5O2 4NO+6H2O K1=1×1053(900℃)
4NO+6H2O K1=1×1053(900℃)
4NH3+3O2 2N2+6H2O K2=1×1067(900℃)
2N2+6H2O K2=1×1067(900℃)
温度较低时以生成 为主,温度高于900℃时,NO产率下降的原因 。
吸收塔中需要补充空气的原因 。
(5)尾气处理时小型化工厂常用尿素作为氮氧化物的吸收剂,此法运行费用低,吸收效果好,不产生二次污染,吸收后尾气中NO和NO2的去除率高达99.95%。其主要的反应为氮氧化物混合气与水反应生成亚硝酸,亚硝酸再与尿素[CO(NH2)2]反应生成CO2 和N2请写出有关反应化学方程式
, 。
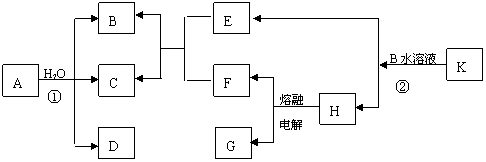

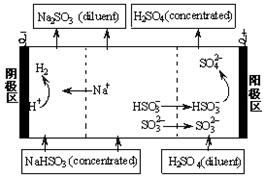 用NaOH溶液吸收二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴阳膜组合循环再生机理如图,则下列有关说法正确的是
用NaOH溶液吸收二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴阳膜组合循环再生机理如图,则下列有关说法正确的是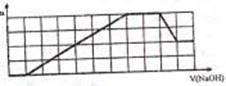 A.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+
A.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+