11、某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等)
|
|
50mL盐酸 |
50mL盐酸 |
50mL盐酸 |
|
m(混合物) |
9.2 g |
15.7 g |
27.6 g |
|
V(CO2)(标况) |
2.24 L |
3.36 L |
3.36 L |
则下列分析推理中不正确的是
A.盐酸的物质的量浓度为3.0 mol/L
B.根据表中数据不能计算出混合物中NaHCO3的质量分数
C.加入混合物9.2 g时盐酸过量
D.15.7 g混合物恰好与盐酸完全反应
 2NaHCO3 Na2CO3+CO2↑+H2O
2NaHCO3 Na2CO3+CO2↑+H2O
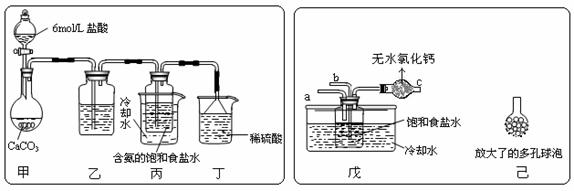
 (Ⅰ)乙装置中的试剂是 ;
(Ⅰ)乙装置中的试剂是 ;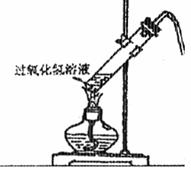 (6分)I、某小组用市售过氧化氢溶液配成15%左右过氧化氢溶液,采用下列装置(装置气密性良好)以过氧化氢代替氯酸钾制取氧气。进行实验。在有不少气泡产生数分钟后,用排空气法收集一试管气体,用带火星的木条检验。
(6分)I、某小组用市售过氧化氢溶液配成15%左右过氧化氢溶液,采用下列装置(装置气密性良好)以过氧化氢代替氯酸钾制取氧气。进行实验。在有不少气泡产生数分钟后,用排空气法收集一试管气体,用带火星的木条检验。 2SO3(g) ;△H < O。 在上述条件下,SO2的转化率约为90%。但是部分发达国家采用高压条件SO3,采取加压措施的目的是
2SO3(g) ;△H < O。 在上述条件下,SO2的转化率约为90%。但是部分发达国家采用高压条件SO3,采取加压措施的目的是 x Mg + Mo3S4
x Mg + Mo3S4  MgxMo3S4
MgxMo3S4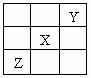 已知X、Y、Z三种主族元素在周期表中的相对位置如图所示,且X的原子序数为a,下列说法不正确的是
已知X、Y、Z三种主族元素在周期表中的相对位置如图所示,且X的原子序数为a,下列说法不正确的是 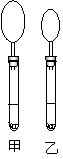 右图是10mLpH均为2的盐酸和醋酸分别与足量的碳酸钙反应一段时间后,所观察到的实验现象(反应过程中产生的气体收集在试管上部的气球中)。
右图是10mLpH均为2的盐酸和醋酸分别与足量的碳酸钙反应一段时间后,所观察到的实验现象(反应过程中产生的气体收集在试管上部的气球中)。