摘要:各地电视台的天气预报中都要报城市的空气质量.根据国家环保局的统一规定.目前进行常规大气监测的项目是:氮氧化合物.二氧化硫.悬浮颗粒物等三种大气污染物. (1)德国科学家曾经利用卫星数据和一种先进的仪器.绘制了一幅地球上空二氧化氮的分布图.从科学家绘制的二氧化氮分布图看.欧洲和北美洲的一些大城市上空二氧化氮密度很高.其原因是什么? . (2)与氮氧化合物有关的全球或区域性大气环境问题涉及到的有 . A.酸雨 B.臭氧层空洞 C.光化学烟雾 (3)为了降低汽车尾气对大气的污染.目前最有效的方法是给汽车安装尾气净化装置.它能将一氧化碳和氮氧化物(NOx)通过催化剂发生反应转化为无害气体.其反应的化学方程式为 . (4)用KIO3一淀粉溶液可定性检验空气中的SO2.写出反应的化学方程式. . (5)高锰酸钾法可定量测定空气中的SO2含量:反应器中有25.00mL 0.0200mol·L-1的酸性KMnO4溶液.往其中持续缓缓通入VL的空气.结束后.溶液仍呈淡红色.此时应用标准还原性溶液反滴定剩余的KMnO4溶液.下列溶液中可作为标准还原性溶液的是 A.FeSO4溶液 B.H2O2溶液 C.KNO3溶液 D.H2C2O4溶液
网址:http://m.1010jiajiao.com/timu3_id_386850[举报]
各地电视台的天气预报中都要预报城市的空气质量。一般将城市空气中的SO2含量和可吸入颗粒的含量(可用g/cm3表示)分为8个等级。目前,测定空气中SO2含量时主要是采用一些氧化还原法。已知:SO2气体与酸性KMnO4溶液反应时,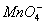 被还原成Mn2+,SO2被氧化成
被还原成Mn2+,SO2被氧化成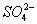 。
。
现有药品:0.1mol/L的酸性KMnO4溶液、颗粒吸附剂、品红试纸、pH试纸。
(1)配置250mL0.1mol/L的酸性KMnO4溶液需要用到的仪器有__________________、__________________、玻璃棒、胶头滴管、烧杯等,玻璃棒的作用是________________和________________。
(2)在测定SO2含量和可吸入颗粒的含量时,首先应测定________________,因为__________________________。
(3)写出SO2与酸性KMnO4溶液反应的离子方程式:_________________________________。
(4)若气体的流速为acm3/min,当tmin时,200mL0.1mol/L的酸性KMnO4溶液恰好完全褪色,则空气中的SO2的含量为___________g/cm3。
查看习题详情和答案>>