4、环己烯常用于有机合成。现通过下列流程,以环己烯为原料合成环醚、聚酯、橡胶,其中F可以做内燃机的抗冻剂,J分子中无饱和碳原子。
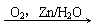 已知:R1-CH=CH-R2
R1-CHO+R2-CHO
已知:R1-CH=CH-R2
R1-CHO+R2-CHO
⑴F的名称是_________,C中含有的官能团的名称是______,H的结构简式为______________。
⑵③的反应条件是____________________。
⑶写出下列有机物的类别:A____________,E___________。
⑷写出下列反应类型:⑥_______________,⑨___________ 。
⑸写出⑩反应的化学方程式: 。
⑹有机物B和I的关系为____________(填序号,多填扣分)
(A)同系物 (B)同分异构体 (C)都属于醇类 (D)都属于烃
 (1)乙二醇;醛基;[ C-C-O-CH2-CH2-O ]n
(1)乙二醇;醛基;[ C-C-O-CH2-CH2-O ]n
(2)NaOH醇溶液、加热 (3)卤代烃;羧酸 (4)氧化;消去



|
(6)C
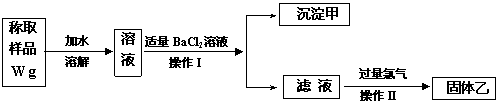 实验室需要制备纯净的氯化钾。现有含少量KBr和K2SO4的氯化钾样品,按照下图所示的实验方案进行提纯。
实验室需要制备纯净的氯化钾。现有含少量KBr和K2SO4的氯化钾样品,按照下图所示的实验方案进行提纯。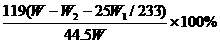 (4)(关键是写出过量K2CO3一步的实验流程,否则不给分)
(4)(关键是写出过量K2CO3一步的实验流程,否则不给分)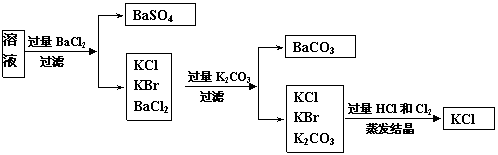
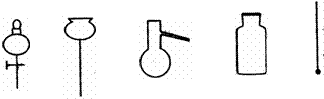
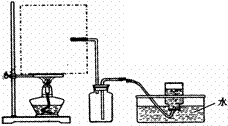 ①从下图挑选所需的仪器,画出Ⅰ中所缺的气体发生装置(添加必要的塞子、玻璃管、胶皮管,固定装置不用画),并标明容器中的试剂。
①从下图挑选所需的仪器,画出Ⅰ中所缺的气体发生装置(添加必要的塞子、玻璃管、胶皮管,固定装置不用画),并标明容器中的试剂。
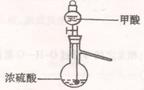 答案:(10分)(1) ①仪器选择正确并标时液体1分,温度计水银球的位置1分②防止水槽中的水因倒吸流入蒸馏烧瓶中(1分)
答案:(10分)(1) ①仪器选择正确并标时液体1分,温度计水银球的位置1分②防止水槽中的水因倒吸流入蒸馏烧瓶中(1分)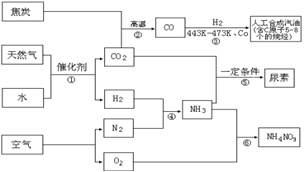 (1)反应③的H2也由反应①得到。若反应①、②、③的转化率均为100%,则将反应①中得到的CO2和H2全部用于合成人工汽油却不能得到理想的产品。
(1)反应③的H2也由反应①得到。若反应①、②、③的转化率均为100%,则将反应①中得到的CO2和H2全部用于合成人工汽油却不能得到理想的产品。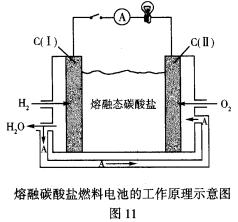 (3)若X与稀硫酸反应生成无色没有气味的气体A,与浓氢氧化钠溶液加热反应生成气体B。等物质的量的A和B在水溶液中反应又生成X。
(3)若X与稀硫酸反应生成无色没有气味的气体A,与浓氢氧化钠溶液加热反应生成气体B。等物质的量的A和B在水溶液中反应又生成X。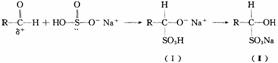 (2)α一氢(R-CH2-CHO)表现出一定酸性,能与碱作用,产生碳负离子:R-–CH-CHO。
(2)α一氢(R-CH2-CHO)表现出一定酸性,能与碱作用,产生碳负离子:R-–CH-CHO。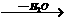 R-CH2-CH=N-NH2,则A的结构简式为
R-CH2-CH=N-NH2,则A的结构简式为
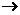 C(分子式:C4H8O2)
C(分子式:C4H8O2)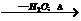 D
D