0 37712 37720 37726 37730 37736 37738 37742 37748 37750 37756 37762 37766 37768 37772 37778 37780 37786 37790 37792 37796 37798 37802 37804 37806 37807 37808 37810 37811 37812 37814 37816 37820 37822 37826 37828 37832 37838 37840 37846 37850 37852 37856 37862 37868 37870 37876 37880 37882 37888 37892 37898 37906 447348
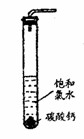 报道了如下实验研究 :
报道了如下实验研究 :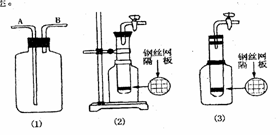 (I)使用常用仪器,运用化学原理进行巧妙的设计,就可以用同一个简单的装置实现多种用途。
(I)使用常用仪器,运用化学原理进行巧妙的设计,就可以用同一个简单的装置实现多种用途。

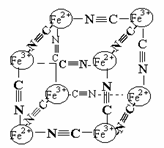 分析化学中常用X射线研究晶体结构.有一种蓝色晶体{可表示为:MxFey(CN)Z
},研究表明它的结构特性是:Fe2+和Fe3+分别占据立方体的点, 自身互不相邻,而CN-位于立方体的棱上.其晶体中的部分离子的空间结构关系如图示,下列说法正确的是
分析化学中常用X射线研究晶体结构.有一种蓝色晶体{可表示为:MxFey(CN)Z
},研究表明它的结构特性是:Fe2+和Fe3+分别占据立方体的点, 自身互不相邻,而CN-位于立方体的棱上.其晶体中的部分离子的空间结构关系如图示,下列说法正确的是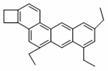 A.2 倍 B.4 倍 C.6
倍 D.36 倍
A.2 倍 B.4 倍 C.6
倍 D.36 倍 2Z(g),若要使平衡时反应物总物质的量与生成物的物质的量相等,且用X、Y作反应物,则X、Y的初始物质的量之比的范围应满足
( )
2Z(g),若要使平衡时反应物总物质的量与生成物的物质的量相等,且用X、Y作反应物,则X、Y的初始物质的量之比的范围应满足
( )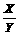 <3
B.
<3
B.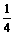 <
<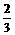 C.3<
C.3<