甲:将锌放入浓盐酸中,反应速率较快
乙:将实验过程记录下来,并交流。
|
|
根据上述资料与交流材料回答下列列问题
⑴乙反应速率明显比甲快,原因是: 。
⑵丙、丁根据铜位于金属活动顺序表氢之后,与盐酸不反应,对乙产生的气体体积比甲大的事实。作出如下推断:
①丙认为是溶解在溶液中的H2逸出,你认为是否有道理,理由是: 。
②丁作了如下猜想,是否成立,请你设计实验方案。
|
丁猜想 |
验证方法 |
预测现象及结论 |
|
丁认为铜片中可能含有锌等杂质 |
|
|
⑶戊注意到乙中(3)中的白色沉淀,分析:不可能是CuCl2,因为CuCl2溶液显蓝色或绿色,也不可能是氯化锌,因为稀释后溶液更稀,不会析出。并利用资料①②大胆猜想,白色沉淀是生成的氯化亚铜。请你帮他设计验证方案(若有多个只设计两个方案):
|
戊 |
预计验证方法 |
预测的现象与结论 |
|
白色沉淀是氯化亚铜 |
|
|
|
|
|
⑷指导老师肯定了戊的猜想,请结合资料③,写出铜与足量浓盐酸在加热条件下反应生成无色溶液及气体,化学方程式可能是: 。
乙的实验步骤(3)稀释,生成沉淀,实际上是一个平衡问题,请写出这一平衡关系:
(用离子方程式表示)。
⑸就铜与浓盐酸反应若进一步探讨,你认为下一步实验方案: 。
 ;
; ;
; ;(每空1分)
;(每空1分)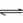 CO32-+H2O HCO3-+OH-、CO32-水解使溶液呈碱性 (每空方程式2分,叙述1分)
CO32-+H2O HCO3-+OH-、CO32-水解使溶液呈碱性 (每空方程式2分,叙述1分)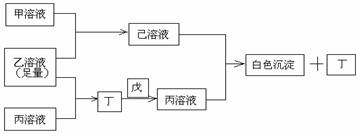
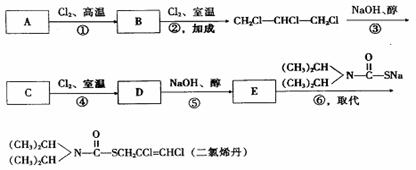
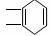 D:CH3CH(OH)CH2COOH
D:CH3CH(OH)CH2COOH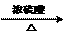 CH3CH=CHCOOCH3 + H2O (主)
CH3CH=CHCOOCH3 + H2O (主)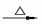 Cu2O(红色)+CH3COOH +2H2O
Cu2O(红色)+CH3COOH +2H2O 4NO+6H2O
4NO十3O2十2H2O=4HNO3
4NO+6H2O
4NO十3O2十2H2O=4HNO3
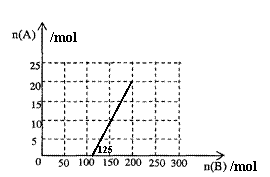 (4)①
(4)① 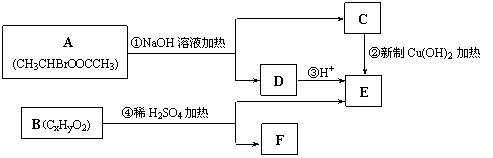
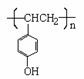

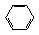
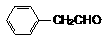
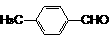
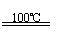
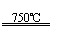
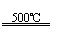
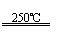 ①CaBr2+H2O CaO+2HBr ②2HBr+Hg HgBr2+H2
①CaBr2+H2O CaO+2HBr ②2HBr+Hg HgBr2+H2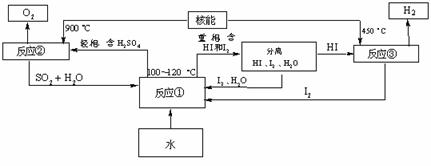 (3)利用核能把水分解,制出氢气,是目前许多国家正在研究的课题。下图是国外正在研究中的一种流程(硫-碘热循环法),其中用了过量的碘。
(3)利用核能把水分解,制出氢气,是目前许多国家正在研究的课题。下图是国外正在研究中的一种流程(硫-碘热循环法),其中用了过量的碘。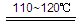 2HI+H2SO4 (2分)SO2和I2可循环使用,无污染。 (2分)
2HI+H2SO4 (2分)SO2和I2可循环使用,无污染。 (2分)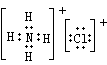 (2)2NH4Cl
(2)2NH4Cl H2↑+Cl2↑+2NH3↑(3)2Fe2+ +Cl2=2Fe3+ +2Cl-
H2↑+Cl2↑+2NH3↑(3)2Fe2+ +Cl2=2Fe3+ +2Cl-