4.在0℃,1.01×105Pa时,分别向甲、乙、丙三个容器中加入30.0mL同浓度的盐酸,再加入不同质量的由两种金属组成的合金粉末,测量放出气体的体积。若在甲、乙、丙三个容器中加入与盐酸同体积同浓度的NaOH溶液,再分别加入与上述实验相同质量的同种合金,测量放出气体的体积,如下表:
|
反应容器 |
甲 |
乙 |
丙 |
|
加入合金质量(g) |
0.510 |
1.53 |
3.57 |
|
与盐酸反应生成气体的体积(L) |
0.560 |
0.672 |
0.672 |
|
与氢氧化钠反应生成气体的体积(L) |
0.336 |
x |
y |
⑴根据表中数据可以计算得出的是 (填字母编号);
A.合金的组成 B.合金中各组分的含量 C.盐酸的物质的量浓度 D.盐酸溶液的密度
能计算出的量的值为 。
⑵若两种金属是下列选项中的某两种金属,则从甲容器中的两次实验来看:
①若不经计算,肯定没有 (填字母编号);
A.40Ca B.56Fe C.64Cu D.24Mg E.27Al
②通过计算讨论合金的成分 。
⑶根据⑵的推测结果,计算x和y的值分别为多少?
 B
B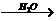 C
C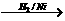 D
D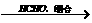 E
E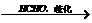 F(
F(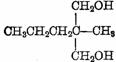 )
)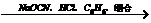 眠尔通
眠尔通 ④
④  -C≡CH ⑤
-C≡CH ⑤
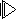 -CH=CH2……
-CH=CH2…… 
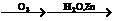 R-CHO+R’-CHO;
R-CHO+R’-CHO;
 聚碳酸酯
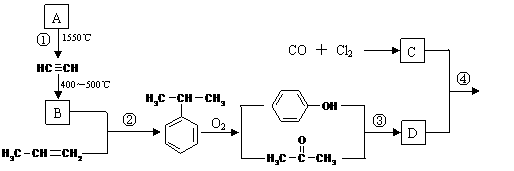
聚碳酸酯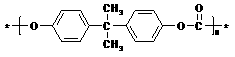 是一种优良的工程塑料,下图表示的是以丙烯和A(“西气东输”工程的主要气态物质)为原料合成该塑料的过程。
是一种优良的工程塑料,下图表示的是以丙烯和A(“西气东输”工程的主要气态物质)为原料合成该塑料的过程。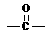 的化合物发生缩合反应,生成新的有机物和水
的化合物发生缩合反应,生成新的有机物和水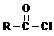 反应生成酯,如:
反应生成酯,如: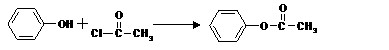 ⑴写出D的结构简式D______________
⑴写出D的结构简式D______________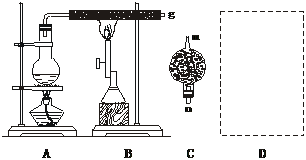
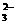 、SO
、SO ,为检验溶液中所含的各阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞试液。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
,为检验溶液中所含的各阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞试液。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。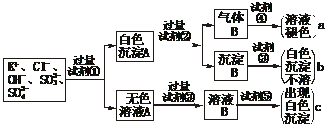
 (6)气体B通入试剂④发生反应的离子方程式是___________________________。
(6)气体B通入试剂④发生反应的离子方程式是___________________________。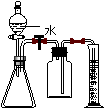 Ⅰ、甲同学将该装置略作改动,设计成了气体溶解度的测量装置。
Ⅰ、甲同学将该装置略作改动,设计成了气体溶解度的测量装置。
 Ⅱ、乙同学将装置略作改动后设计了空气中氧气的体积分数测定装置。
Ⅱ、乙同学将装置略作改动后设计了空气中氧气的体积分数测定装置。